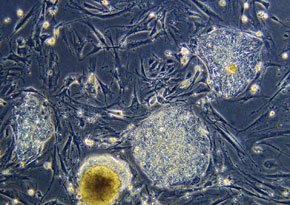
University of Wisconsin / MadisonCTEs humanas: mais difíceis de manipular do que as células de camundongosUniversity of Wisconsin / Madison
As células-tronco, capazes de originar diferentes tecidos do organismo, conquistaram o interesse dos cientistas e da população por representarem uma promessa de tratamento para problemas de saúde ainda sem uma terapia satisfatória. Testes conduzidos em diferentes países nos últimos anos confirmam a versatilidade dessas células – em especial, das células-tronco embrionárias (CTEs), extraídas do embrião dias após sua formação – e contribuem para o surgimento de uma onda de otimismo que, por ora, ainda parece exagerado.
Quanto mais se estudam essas células, mais se descobre que ainda há muito a avançar antes de usá-las em novas terapias. “Teria receio de injetar células-tronco embrionárias em meu corpo e mais receio ainda de usar as células-tronco de pluripotência induzida (iPS), sobre as quais pairam muitas questões sem resposta”, diz Joshua Brickman, do Centro de Medicina Regenerativa da Universidade de Edimburgo, na Escócia. “Temos de continuar os estudos”, afirma ele. Brickman esteve no Brasil em março cuidando dos acertos da quarta edição do curso “Embryonic stem cells as a model system for embryonic development”, que deverá ocorrer em 2013 no Centro de Estudos do Genoma Humano da USP.
Com uma parte teórica e outra prática, o curso reúne as maiores autoridades do mundo no estudo de células-tronco com pesquisadores em início de carreira durante três semanas. Brickman e Jennifer Nichols, pesquisadora do Centro de Estudos sobre Células-tronco da Universidade Cambridge, Inglaterra, o desenvolveram sete anos atrás para treinar jovens pesquisadores da América Latina. Itinerante em suas primeiras edições, o curso já foi ministrado no Chile, no México e no Brasil. Agora Brickman e Jennifer pretendem estabelecer uma base permanente em um desses países.
A seguir, leia os principais trechos da entrevista em que falaram à Pesquisa FAPESP sobre o curso e sobre as questões em aberto a respeito do funcionamento das CTEs.
Por que não sabemos como manter a pluripotência das CTEs no laboratório?
Joshua – A pluripotência é uma definição baseada nas funções das células. Nós não sabemos realmente o que ela é. Meu laboratório trabalha com a questão da pluripotência versus totipotência. Sabemos que algumas células do embrião vão originar todo tipo de célula. O problema é que não sabemos quais células exibem essa propriedade até fazermos um experimento. Agora temos marcadores de CTEs. Mas, mesmo com eles, não podemos ter certeza de que as células que pegamos são CTEs.

eduardo cesarJoshua Brickmaneduardo cesar
A população de CTEs é, portanto, heterogênea?
Joshua – Foi descoberto algo interessante recentemente. Você pega uma placa de Petri com CTEs, escolhe uma célula, testa-a para plutipotência e descobre que ela não faz algo. Não pode se tornar um embrião. Então, você clona essa célula in vitro e obtém outra população de células heterogêneas. De novo, você pega uma célula dessa nova população e descobre que ela pode gerar linhagens embrionárias. A heterogeneidade de uma população de células parece ser importante para que haja CTEs pluripotentes. Não é uma única célula que perpetua a pluripotência. Isso é obtido por um mix complexo de células. A coisa interessante sobre os mamíferos é que você pega uma população de células do embrião em estágio bem inicial e, se corta as células ao meio, consegue dois embriões normais. As células são muito reguladoras. Elas podem regenerar as células que necessitam ter a seu lado no embrião, regenerar esse nicho. Num certo sentido, fazemos um miniexperimento evolutivo quando selecionamos uma célula que pode gerar uma linhagem de células embrionárias.
Jennifer – Discutimos essa questão com pessoas que trabalham com pluripotência. Elas dizem que as CTEs precisam ser homogêneas, têm de estar todas na mesma condição. O sonho seria que todas as células da população de CTEs fossem pluripotentes e se pudesse pegar qualquer uma delas. Mas não concordamos com essa visão.
Joshua – Ainda prevalece a mentalidade de que há uma receita de bolo com a qual se criariam CTEs totalmente iguais, que poderiam se transformar em todos os tecidos. Não há só um tipo de CTEs, mas sim múltiplos. As pessoas que estudam a natureza das CTEs já sabem disso, mas muita gente que está, por exemplo, tentando usar CTEs para produzir células beta do pâncreas para fabricar insulina não sabe.
Jennifer – As CTEs são um modelo de desenvolvimento dos mamíferos. Achamos que os biólogos que melhor entendem as CTEs são os evolucionistas. Se você não entende o desenvolvimento do embrião, não consegue pensar de maneira correta.
Muitos dos experimentos com CTEs são feitos com células de ratos ou camundongos. Por que é mais difícil trabalhar com CTEs humanas?
Jennifer – Porque a embriologia delas é distinta. As células humanas estão num estágio mais avançado de desenvolvimento que as de camundongo e, por isso, não conseguimos explorar suas potencialidades. Voltamos à questão do desenvolvimento. Quando as primeiras CTEs humanas foram obtidas em laboratório, percebeu-se que precisavam de condições diferentes. Eram mais difíceis de cultivar do que as de camundongos. Na verdade, elas eram um tecido diferente. A expressão de marcadores era diferente. Hoje sabemos que as CTEs humanas estão mais próximas das chamadas células-tronco do epiblasto [que vão gerar a pele e o tecido nervoso] derivadas após a implantação do embrião nos camundongos. As CTEs humanas estão no estágio denominado primed pluripotency (não diferenciadas, mas encaminhadas para esse processo), enquanto as CTEs de camundongos estão no de pluripotência naïve (mais imatura).
Joshua – Provavelmente é uma questão de tempo até termos CTEs humanas com as quais poderemos trabalhar como fazemos com as de camundongos.
Jennifer – Há muito trabalho sendo feito. Mas, no caso das CTEs humanas, é possível que não se consiga nunca deixá-las no mesmo estágio das CTEs de camundongo.
Joshua – Não sabemos se isso é possível. Ainda precisamos fazer experimentos. Houve tentativas de fazer isso, mas tiveram um sucesso limitado.

eduardo cesarJennifer Nicholseduardo cesar
Seria o caso de a pesquisa se concentrar mais em CTEs humanas e menos nas de camundongos?
Jennifer – Sem os estudos com as células de animais não saberíamos nem por onde começar o trabalho com as células humanas. Não saberíamos que seria possível obter todas essas linhagens num meio de cultura.
Joshua – Para fazer genética de verdade, é preciso ter células humanas como as dos camundongos, capazes de serem manipuladas. As células dos camundongos podem sofrer alterações genéticas específicas e gerar linhagens celulares, a partir das quais são obtidas múltiplas gerações com essas alterações. Esses experimentos são vitais. Podemos modificar uma célula de camundongo. Você pode transformar CTEs de camundongos em células do epiblasto, que são muito mais próximas das CTEs humanas. Essa abordagem pode ser muito produtiva. Não dá para manipular dessa forma as CTEs humanas. É preciso trabalhar tanto com as CTEs humanas como as de camundongos. Não sabemos de onde virá a inovação.
Vocês acreditam que a imprensa e os próprios cientistas criaram expectativas exageradas sobre as possibilidades terapêuticas das CTEs, mais ou menos como ocorreu com a questão do sequenciamento do genoma humano?
Joshua – É preciso fazer uma distinção. Temos terapias baseadas no transplante de células-tronco [adultas, extraídas da medula dos ossos] há 30 anos. Mas eu concordo que houve um exagero. Os cientistas são os responsáveis por promover uma expectativa realista sobre as pesquisas. Mas muitos estão mais preo-cupados em conseguir atenção da imprensa e financiamento para suas pesquisas com base em promessas. No Reino Unido há uma linha de financiamento no Conselho de Pesquisa Médica que, inicialmente, estimulava testes clínicos cinco anos depois da pesquisa básica. Isso é irreal e também ocorre em outras áreas. Mas há esperança em alguns lugares. Um inglês, Peter Coffey, está usando CTEs para tratar degeneração macular. Isso é muito excitante. Mas vamos curar Parkinson ou distrofia muscular amanhã? De jeito nenhum. Temos de ser realistas. Esses são objetivos para 20 ou 30 anos. E pode ser que toda a pesquisa com CTEs não leve a nenhuma terapia celular. Mas talvez possamos identificar fatores que as células produzem e que podem ser usados para estimular o reparo endógeno do organismo, algo muito mais excitante. Acho que as áreas em que vamos usar CTEs são aquelas em que hoje já se têm protocolos usando células adultas, como leucemia ou diabetes do tipo 1 [transplantes de células do pâncreas de cadáveres]. Isso não vai acontecer amanhã. Talvez daqui a 5 ou 10 anos. Não vamos curar todas as doenças com CTEs.
E as pesquisas com células-tronco de pluripotência induzida (iPS)?
Joshua – Cinco ou seis anos atrás, muita gente pulou da pesquisa com CTEs para iPS. Hoje vejo que eles estão fazendo as mesmas perguntas que eu. Eles apenas mudaram o modelo de estudo. As iPS não são a mesma coisa que as CTEs. São feitas muitas mudanças nas células adultas para que virem iPS, para que regridam a esse estágio. Quando células diferenciadas a partir de iPs são colocadas em modelos animais, há uma chance maior de gerar tumores. Não vamos esquecer que o câncer é uma transformação e as iPS são células geneticamente transformadas. As CTEs podem ter um fenótipo similar ao de um câncer, mas são geneticamente normais. Uma célula iPS não é mais geneticamente normal, foi transformada. Teria receio de injetar células-tronco embrionárias em meu corpo e mais receio ainda de usar as iPS, sobre as quais pairam muitas questões sem resposta Por isso é importante não parar as pesquisas com CTEs só porque as células iPS estão disponíveis.
Jennifer – Voltamos à questão de como diferenciar as CTEs humanas. As iPS não são tão boas quanto se gostaria que fossem. Mas acho que representam uma linha de pesquisa fantástica.
Por que vocês gostariam de estabelecer uma base permanente do curso sobre CTEs no Brasil?
Joshua – Eu e Jennifer fazemos esse curso, baseado nos moldes do que é dado em Cold Spring Harbor [nos Estados Unidos], há sete anos, sempre em lugares diferentes. Mas agora temos interesse em criar uma base permanente. Assim, seria mais fácil administrá-lo. Para trazer os pesquisadores de fora, precisamos de estrutura e investimento. São Paulo tem os recursos, as instalações e as pessoas para fazer isso. Só se pode fazer o curso num lugar onde há pesquisa, pois é uma relação de mão dupla. A pesquisa ajuda o curso e o curso ajuda a pesquisa. Não há muitos lugares assim.
Jennifer – As pessoas temem que, se montarem uma estrutura para o curso e as coisas derem errado, não saberão lidar com isso. Digo o seguinte: sim, as coisas dão errado. Mas você vai lá e conserta. As coisas não são tão complicadas assim. Além de nós dois, que iremos visitar o lugar do curso ao menos a cada dois anos, vamos trazer outras pessoas. E poderemos ser contatados a qualquer momento pelos alunos.
Joshua – Tivemos uma reunião com alunos da professora Mayana Zatz, do Centro de Estudos do Genoma Humano da USP, e o nível de entusiasmo é impressionante. Na Europa, não se vê isso. Não se pode esquecer que, além do Brasil, alunos da América Latina e da Europa vão participar do curso. Esses alunos acabam criando uma rede de colaboração internacional, visitam-se mutuamente e serão os chefes de departamento nas universidades daqui a algum tempo. Vamos treinar não apenas alunos de doutorado, mas também jovens professores.
O que vocês ensinam no curso? A diferenciar CTEs?
Jennifer – Essa é uma parte pequena do curso. O mais importante é que os alunos estabeleçam conexões, que eles saibam o que é possível fazer. Claro que tentamos ensinar coisas práticas. Mas eles não se tornarão perfeitos nessas tarefas. Eles irão fazer as coisas, algo dará errado, mas eles podem contar com seus contatos do curso para resolver os problemas. Gostamos de imaginar que ensinamos os alunos a pensar criticamente. Eles são alvo de bullying nosso, do Josh.

