O Brasil dá os primeiros passos na corrida por um mercado que tem atraído dezenas de milhões de dólares nos últimos anos, o de produtos alternativos à carne bovina, mas com as mesmas características sensoriais dela. Existem duas rotas para se alcançar esse objetivo: a produção de carne em laboratório a partir de células-tronco de animais, também conhecida como carne limpa ou in vitro, e a criação de um produto à base de proteínas vegetais que emule a carne vermelha. Em maio deste ano, o empreendedor carioca Marcos Leta colocou no mercado o Futuro Burger, um hambúrguer vegetal que promete ter a aparência e o gosto de carne bovina. Fundador dos sucos Do Bem, o empresário é dono da foodtech Fazenda Futuro, responsável pela novidade, vendida, por enquanto, em lanchonetes e supermercados selecionados de São Paulo, Rio de Janeiro e Minas Gerais, por volta de R$ 17 a bandeja com duas unidades.
Leta segue o caminho trilhado por empresas estrangeiras que já comercializam alternativas vegetais ao produto de origem animal, conhecidas no mundo como plant-based meat (carne feita de plantas). A base de ingredientes do Futuro Burger é formada por proteína isolada de soja, de grão-de bico e de ervilha. A cor avermelhada é conferida por suco de beterraba. Segundo Leta, não é só na aparência que o alimento é parecido com a carne de origem animal. “O Futuro Burger tem sabor, textura e aroma idênticos ao da carne vermelha, além de um valor nutricional muito similar”, diz.

Futuro Burger/Divulgação
Marcos Leta, do Futuro Burger, desenvolveu um produto à base de vegetais que reproduz a carne vermelhaFuturo Burger/DivulgaçãoEsse resultado foi obtido por meio da análise, com a ajuda de inteligência artificial, das melhores combinações de proteínas e lipídeos de origem vegetal. Também foi utilizada uma língua artificial, equipamento eletrônico composto por sensores gustativos que imitam o funcionamento do órgão humano.
Vegetarianos não são o único alvo das empresas que investem na fabricação de carne à base de plantas. O objetivo é atingir quem busca se alimentar de forma mais saudável e ecologicamente sustentável. Estudo divulgado pelo Observatório do Clima, em 2016, mostrou que o setor agropecuário responde por 69% das emissões de gases de efeito estufa no Brasil. “Ao desenvolvermos tecnologias capazes de criar alimentos idênticos à carne que não derivam de animais, queremos mostrar que é possível revolucionar a indústria alimentícia sem gerar impactos negativos no ambiente”, destaca o dono da Fazenda Futuro.
No desenvolvimento do projeto, a startup teve consultoria da organização The Good Food Institute (GFI), fundada nos Estados Unidos há três anos com o objetivo de promover o desenvolvimento de proteínas alternativas. “Trabalhamos para criar um sistema de alimentos mais sustentável, saudável e justo. Nosso time de cientistas, empreendedores, advogados e especialistas em políticas públicas trabalham para que a indústria de alimentos passe a usar produtos feitos de plantas ou de células de animais”, explica Felipe Krelling, coordenador de inovação e pesquisas do GFI no Brasil.
Mercado concorrido
Novidade no Brasil, o hambúrguer vegetal que imita carne bovina já existe há três anos nos Estados Unidos. A Beyond Burger foi a primeira empresa a ter seu hambúrguer à base de plantas vendido em redes de supermercados naquele país, em maio de 2016. Este ano, tornou-se a primeira fabricante de carne vegetal a ter ações na bolsa norte-americana Nasdaq e pode se transformar rapidamente em um unicórnio do setor de alimentos, ou seja, alcançar valor de mercado igual ou superior a US$ 1 bilhão. Além de hambúrguer, ela vende carne moída e salsicha preparadas mediante uma combinação de fontes proteicas vegetais.
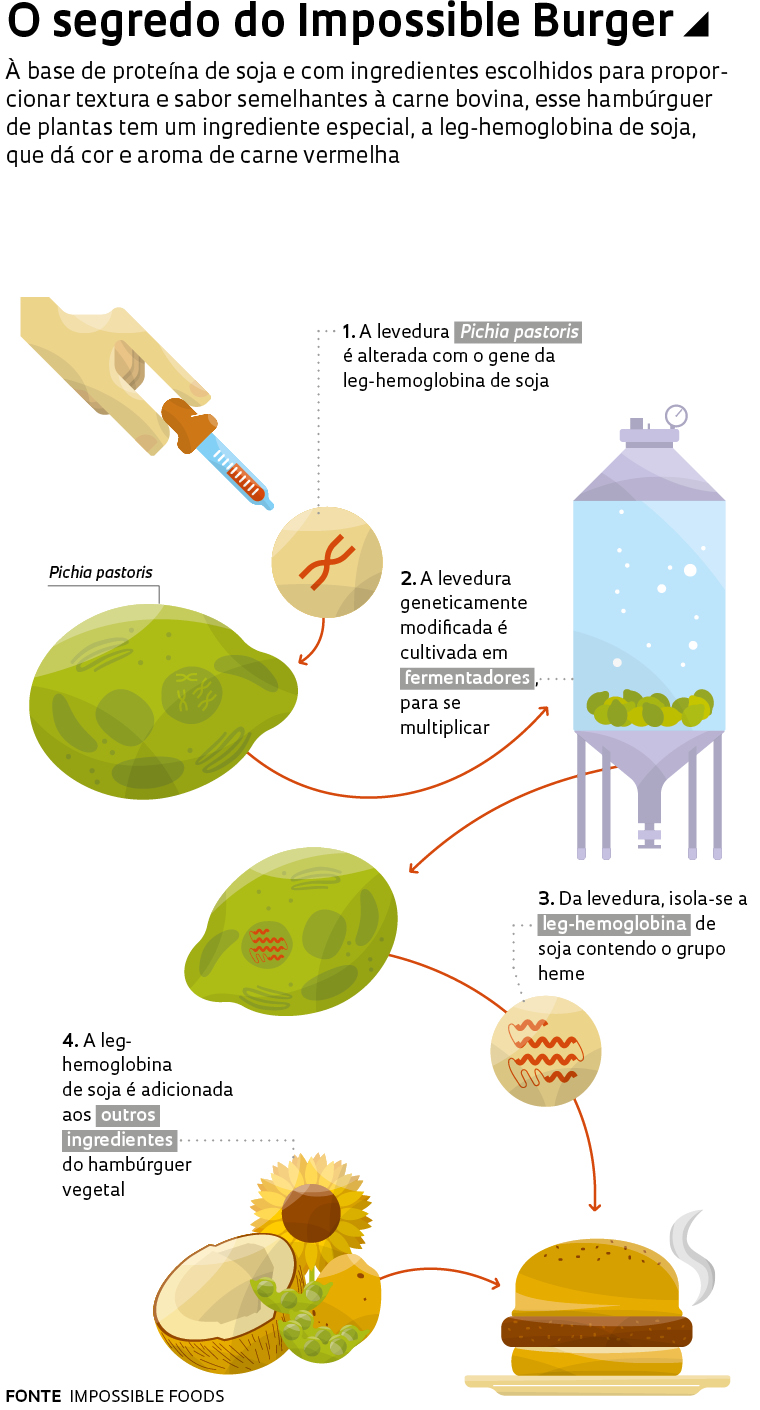
Já a startup californiana Impossible Foods deu um passo além. A cor vermelha de seu Impossible Burger não vem da adição de beterraba, mas de uma proteína similar à hemoglobina, produzida por engenharia genética. Seus pesquisadores descobriram que é um componente da hemoglobina, o grupo heme, que confere a cor vermelha à carne crua e o cheiro característico exalado durante o cozimento. Raízes de plantas leguminosas, como a soja, também têm o grupo heme em uma proteína de estrutura e função muito semelhante à hemoglobina, a leg-hemoglobina.
Com base nesse conhecimento, os cientistas da Impossible Foods desenvolveram um método de produção em alta escala do grupo heme, extraindo-o de raízes da soja e propagando-o em laboratório. Por meio de engenharia genética, eles modificaram um tipo de levedura (Pichia pastoris) para que ela produzisse leg-hemoglobina de soja e a cultivaram em fermentadores para multiplicar a proteína. Assim, obtiveram um ingrediente que, além de acrescentar cor e aroma de carne ao produto, ainda o enriquece com ferro.

Impossible Foods/Divulgação
Fábrica da startup californiana Impossible FoodsImpossible Foods/DivulgaçãoHambúrguer in vitro
Os empreendedores que investem no cultivo de células-tronco de bovinos para criar carne sintética, também chamada de cell-based meat (carne feita de células), têm um argumento ainda mais contundente para atrair os amantes de um bom bife: o que eles fazem não é simplesmente algo parecido com carne, mas a própria carne – só que obtida sem o sacrifício de animais. O primeiro hambúrguer in vitro nasceu na Universidade de Maastricht, na Holanda, a partir das pesquisas do professor de fisiologia vascular Mark Post.
Os estudos se iniciaram em 2008 e o resultado foi apresentado ao mundo cinco anos depois durante uma coletiva de imprensa realizada em Londres. Naquela ocasião, três pessoas que provaram o hambúrguer – o próprio Post e dois especialistas em gastronomia e ciência de alimentos – concordaram que a carne estava um pouco seca e pobre em sabor, devido à falta de gordura na composição, segundo cobertura feita pelo jornal The New York Times.
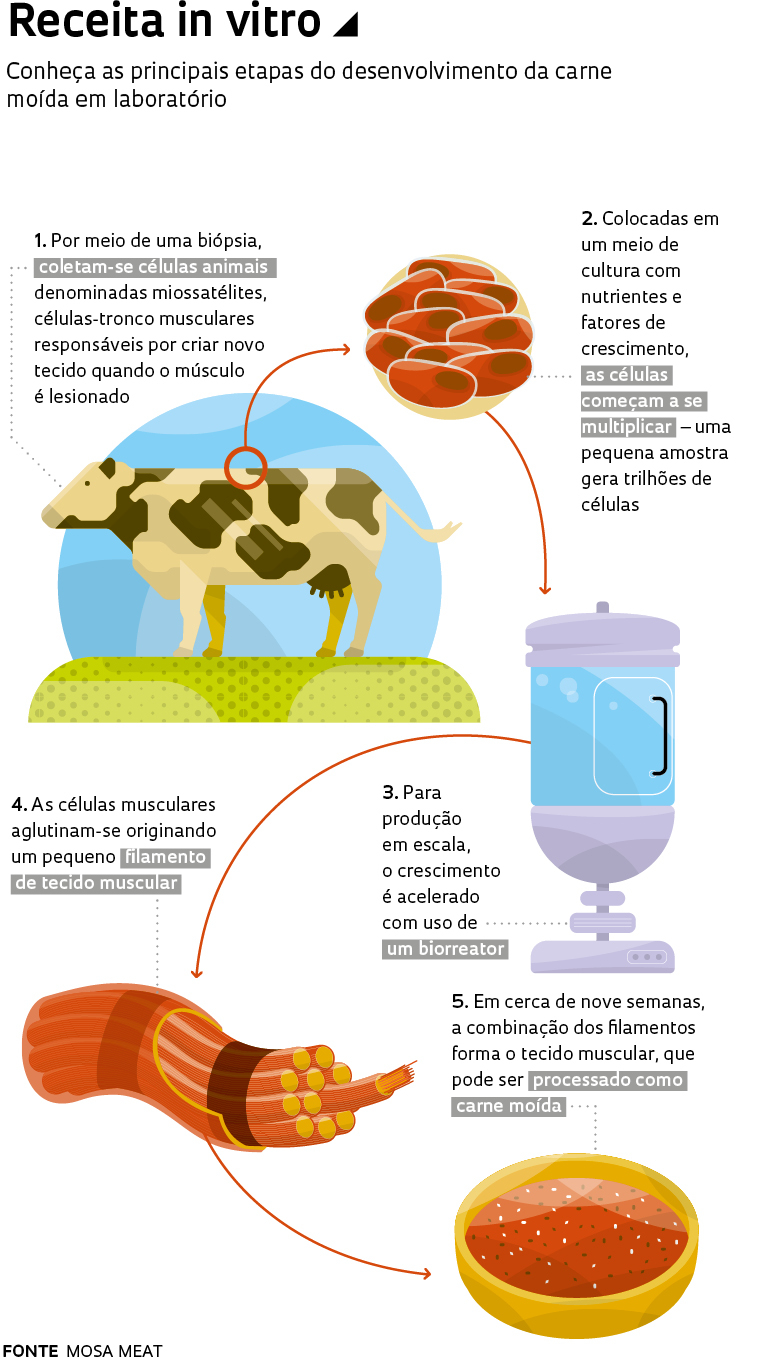
O processo desenvolvido por Post parte da extração de células-tronco bovinas de um fragmento de tecido muscular do animal. Essas células indiferenciadas multiplicam-se em um meio de cultura contendo nutrientes e fatores de crescimento, transformando-se em fibras musculares. Cerca de 20 mil finas tiras de tecido muscular combinam-se para formar um hambúrguer com cerca de 140 gramas. A produção em escala industrial será feita dentro de um biorreator, um aparelho similar ao utilizado para a fermentação de leveduras (ver infográfico).
O hambúrguer holandês não saiu barato. Custou € 250 mil (R$ 1,1 milhão), financiados principalmente por Sergey Brin, cofundador do Google. Para colocar o produto no mercado, o pesquisador criou a empresa Mosa Meat, nascida como uma spin-off da Universidade de Maastricht. Em julho de 2018, para continuar o desenvolvimento do produto e iniciar sua comercialização, a startup captou € 7,5 milhões do Bell Food Group, líder no mercado de carnes na Suíça, e da holandesa M Ventures, braço corporativo de capital de risco da farmacêutica alemã Merck.

Mosa Meats/Divulgação
O holandês Mark Post foi o responsável pelo primeiro hambúrguer in vitroMosa Meats/DivulgaçãoMark Post declarou, por meio de sua assessoria de imprensa, que tem interesse em vender seu produto no continente americano, “especialmente na América do Sul, onde o consumo de carne é tão alto”. Ele já visitou o Brasil e recentemente esteve na Colômbia, onde se reuniu com produtores de carne. A expectativa é que o hambúrguer da Mosa Meat chegue ao mercado em 2021.
Novidade israelense
No final do ano passado foi a vez da israelense Aleph Farms anunciar ter criado o primeiro bife cultivado em laboratório. Didier Toubia, CEO da empresa, contou para Pesquisa FAPESP que a decisão de pesquisar carne cultivada a partir de células animais surgiu em 2016, durante uma reunião com a incubadora The Kitchen Hub, pertencente ao Grupo Strauss, fabricante de alimentos de Israel. O projeto se concretizou na Faculdade de Engenharia Biomédica do Instituto de Tecnologia de Israel (Technion).
O custo do protótipo, uma pequena tira de bife de algumas dezenas de gramas, foi de US$ 50, valor ainda bastante alto quando comparado ao da carne vendida em açougues, mas um avanço em relação ao despendido para a produção do hambúrguer de Maastricht. Sobretudo considerando-se o fato de que fazer um bife no laboratório é mais complicado do que produzir carne moída para hambúrguer. A novidade da startup israelense deve chegar ao mercado em até cinco anos.
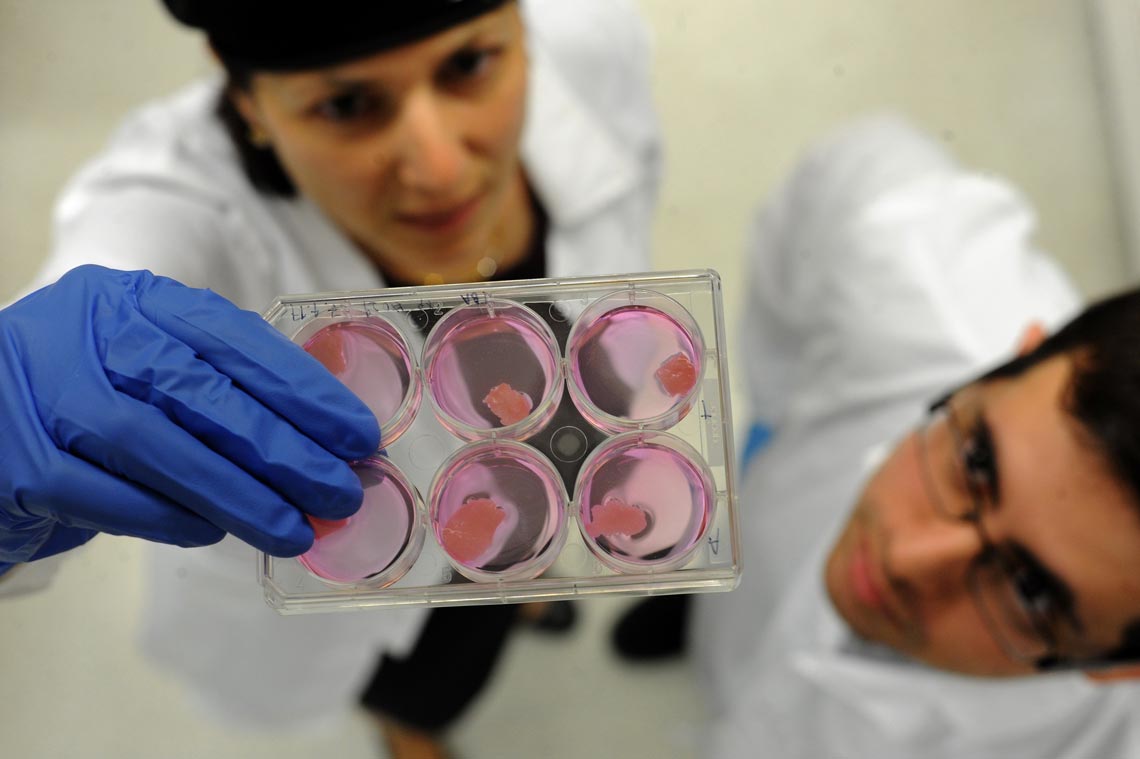
Aleph Farms/Divulgação
Equipe de pesquisa e desenvolvimento da israelense Aleph Farms, que em 2018 anunciou o primeiro bife cultivado em laboratórioAleph Farms/DivulgaçãoO processo de produção de um bife in vitro requer que as células se organizem de forma tridimensional (3D), ganhando volume e, consequentemente, espessura. No entanto, quando células são cultivadas dentro de uma placa de cultura, elas proliferam em uma única camada. Para que formem camadas sobrepostas, ganhando contornos tridimensionais, é necessário colocá-las em uma estrutura que serve como suporte denominada scaffold (andaime, em inglês).
Em laboratórios e companhias voltados a projetos de medicina regenerativa é comum o uso de scaffolds produzidos a partir de colágeno, produto de origem animal. Mas para fabricar carne limpa é importante garantir que não exista nenhum insumo ou procedimento vinculado ao sofrimento de animais e aos métodos tradicionais de abate. Esse pré-requisito tem gerado impacto em toda a cadeia de produção da carne limpa e estimulado o desenvolvimento de novas tecnologias auxiliares e o surgimento de empresas voltadas à produção dessas ferramentas. Uma das startups criadas para fornecer scaffolds à base de plantas a essa indústria é a brasileira Biomimetic Solutions, uma spin-off nascida no Centro Federal de Educação Tecnológica de Minas Gerais (Cefet-MG).
“Criamos um polímero sintético à base de plantas. Somos uma das primeiras empresas no mundo especializada na produção de scaffolds com foco na produção de carne limpa”, afirma Lorena Viana, mestranda em inovação pela UFMG e uma das fundadoras da startup, juntamente com as engenheiras de materiais Ana Elisa Antunes e Alana Benz, ambas formadas no Cefet-MG, e duas pesquisadoras da instituição, Aline Bruna da Silva e Roberta Viana.
Ao criar a empresa, em 2016, o plano das sócias era trabalhar na produção de pele humana artificial. Mas, no ano seguinte, a startup participou de um programa da aceleradora britânica RebelBio e resolveu apostar na inovação, mudando seu foco de atuação. “Decidimos focar nosso negócio no mercado de carne in vitro, no qual temos poucos concorrentes diretos”, ressalta Viana, que atua como diretora comercial do negócio. Mosa Meat e Aleph Farms já desenvolvem seus próprios scaffolds, e há pesquisas com esse objetivo em universidades norte-americanas e canadenses.

Biomimetic Solutions/Divulgação
A empresa mineira Biomimetic Solutions fornece a base vegetal para a fabricação de carneBiomimetic Solutions/DivulgaçãoDesafios à vista
O desenvolvimento da carne cultivada a partir de células animais insere-se em um campo mais amplo, conhecido como agricultura celular, que inclui também a elaboração de lácteos, ovos, peixes, couro, seda e até chifres in vitro. A fim de divulgar e impulsionar a agricultura celular no mundo, foi criada nos Estados Unidos em 2016 a Sociedade de Agricultura Celular (CAS).
O brasileiro Matheus Saueressig, aluno de ciências da computação na Universidade Federal do Rio Grande do Sul (UFRGS), é o diretor de comunicações da CAS na América do Sul. “Em todo o mundo, apenas a América Latina ainda não desenvolveu projetos de carne in vitro”, diz ele. “O Brasil é o maior processador de proteína animal do mundo, mas corre o risco de perder esse novo mercado que está surgindo e crescendo rapidamente”, alerta.
Startups dedicadas à pesquisa e à fabricação de carne limpa, segundo Saueressig, vêm recebendo grandes investimentos de empresas de capital de risco, de bilionários, como Richard Branson e Bill Gates, que têm participação na Memphis Meat, com sede na Califórnia, e de multinacionais do setor alimentício – entre elas Cargill, Bell Food Group e Tyson Foods, uma das principais produtoras de carne dos Estados Unidos. Ao investir nos novos fabricantes de carne limpa, os grandes processadores de carne bovina estão preocupados com o futuro. Querem colocar um pé nesse mercado para não ficarem fora dele caso o negócio dê certo.
Por enquanto, as alternativas vegetais dominam o promissor mercado de possibilidades à carne bovina. A norte-americana Associação de Alimentos Baseados em Plantas já tem 140 membros. Um estudo da consultoria Nielsen revelou que os norte-americanos gastaram US$ 670 milhões em carnes de origem vegetal no primeiro semestre de 2018 – veganos e vegetarianos representam apenas 5% da população do país. Negócios dedicados à produção de carnes baseadas em células-tronco miram um mercado bem maior. A carne bovina deverá ser responsável por uma receita de US$ 2,1 trilhões em todo o mundo até 2020, conforme a consultoria norte-americana Grand View Research.
Apesar das boas perspectivas, as startups de carne in vitro já enfrentam reação do mercado. A Associação de Pecuaristas dos Estados Unidos pleiteou ao Departamento de Agricultura que produtos não derivados de animais criados ou abatidos sejam impedidos de ser descritos como bife ou carne – com isso, querem diferenciar o alimento que fabricam da novidade que está entrando no mercado. O maior desafio dessas empresas, no entanto, não é comercial, mas científico. Em primeiro lugar, elas precisam garantir que o processo de produção não faça uso de nenhum componente de origem animal.
No primeiro hambúrguer in vitro, o holandês Mark Post usou soro bovino fetal para nutrir as células-tronco, material comumente empregado como suplemento em meio de cultura. Esse nutriente é obtido do sangue de fetos retirados de vacas prenhes no momento do abate. Hoje, tanto a Mosa Meat quanto a Aleph Farms garantem que não utilizam mais ingredientes derivados de animal.
“Um meio de crescimento destina-se a reproduzir o ambiente celular que existe no interior do animal e deve incluir os mesmos aminoácidos, proteínas, açúcares, vitaminas e fatores de crescimento encontrados no sangue animal. A maioria desses ingredientes deverá ser isolada das plantas e parte deles poderá ser produzida por leveduras”, diz Didier Toubia, da Aleph Farms.
Para o médico veterinário Flávio Vieira Meirelles, professor da Faculdade de Zootecnia e Engenharia de Alimentos da Universidade de São Paulo (USP), essa não é uma tarefa fácil. “Existem, atualmente, alternativas ao soro fetal. Uma das mais comuns é a albumina de soro bovino, que também é um produto de origem animal. E ainda há várias outras substâncias retiradas de animais envolvidas nas diferentes etapas do processo. Acredito que ainda vá levar um tempo até que se consiga fazer cultivo celular em escala industrial com um custo viável que seja completamente livre de produtos de origem animal”, avalia o especialista.
As empresas também investem esforços para que o processo de obtenção de células-tronco seja o menos incômodo possível para o animal. “Acreditamos que os flexitarianos [pessoas que privilegiam dieta vegetariana, mas se permitem comer carne ocasionalmente] serão os primeiros a comprar nossa carne, mas não vemos razão para os vegetarianos não a comprarem. Encontramos uma maneira de isolar as células de uma vaca sem ferir os animais”, afirma Toubia. Como isso é feito, ele não revela. “É segredo.”
Para algumas foodtechs, como as norte-americanas Just e Memphis Meats, produzir carne em laboratório sem gerar incômodo ao animal, nem mesmo uma simples biópsia, não é mais uma possibilidade remota. Elas estão desenvolvendo a produção de carne de frango a partir de células-tronco coletadas de penas do animal. A Just entrou no mercado em 2011, inicialmente com o nome de Hampton Creek, e comercializa alimentos vegetais alternativos aos de origem animal, como maionese. A Memphis Meats, por sua vez, dedica-se à pesquisa de diversos tipos de carne em laboratório, incluindo frango e pato.
Liz Specht, diretora associada de Ciência e Tecnologia do GFI nos Estados Unidos, comeu carne de pato (feita de células) da Memphis Meat, em 2017. “O que mais me impressionou foi a textura do produto. Quando você morde fibras musculares, percebe-se uma elasticidade própria, e a carne baseada em células que provei tinha exatamente a mesma qualidade”, contou ela logo depois da experiência, segundo informou a própria GFI. “A carne foi muito bem preparada. Estava empanada e tinha um molho. Por isso, foi um pouco difícil avaliar o sabor da carne em si, mas a textura era inconfundível.”
Segurança e qualidade
Outro desafio dos fabricantes de carne in vitro é provar que o produto final seja absolutamente seguro ao consumo humano. “Os fabricantes terão que identificar claramente quais as substâncias empregadas no processo de diferenciação celular, comprovando a segurança e a qualidade nutricional”, pondera a bioquímica Viviane Abreu Nunes Cerqueira Dantas, professora do curso de biotecnologia da Escola de Artes, Ciências e Humanidades (EACH) da USP. Doutora em biologia molecular, Viviane pesquisou a produção de pele in vitro a partir de célula-tronco do cordão umbilical, em projeto financiado pela FAPESP entre 2013 e 2016 (ver Pesquisa FAPESP no 245).
Ela também vê com desconfiança a afirmação, comum entre as startups do setor, de que a carne de laboratório, ao contrário do produto oriundo de abate, dispensa o uso de antibióticos. “Considero que a produção de carne em laboratório, em grande escala, não poderá prescindir, em um primeiro momento, do uso de antibióticos para o cultivo das células. Desconheço, entretanto, quais outras substâncias estariam sendo usadas com esse mesmo efeito no contexto da produção da carne in vitro”, avalia a pesquisadora. Ela ressalta que os produtos cárneos, particularmente aqueles que passam por maior manipulação, constituem um excelente meio de cultura de microrganismos devido à elevada umidade, ao pH próximo da neutralidade e à composição rica em nutrientes.
Felipe Krelling, coordenador de Inovação e Pesquisas da GFI, informa que antibióticos podem ser utilizados por um período curto para minimizar riscos de contaminação ao separar uma linha celular de uma biópsia, caso ela já estivesse contaminada por alguma bactéria. “Não há nenhuma necessidade de se utilizar antibióticos em qualquer outro processo de produção. Já existe tecnologia na indústria de bioprocessos que pode ser adotada por empresas cell-based para se obter um ambiente totalmente livre da necessidade de uso de qualquer antibiótico para a proliferação de células”, declara Krelling.
Até mesmo as carnes de base vegetal sofrem questionamentos. Novos ingredientes, como o grupo heme do Impossible Burger, precisam conquistar a confiança do consumidor, e a maior premissa em favor desses produtos – a sustentabilidade ambiental – precisa ser comprovada. Estudo conduzido em 2018 por pesquisadores da Universidade de Michigan, dos Estados Unidos, a pedido da norte-americana Beyond Meat, comparou o impacto ambiental do vegetal Beyond Burger com um hambúrguer de carne bovina. O estudo concluiu que a carne vegetal utiliza 99% menos água, 93% menos terra, gasta 46% menos energia e emite 90% menos gases de efeito estufa.
A edição impressa de julho traz uma versão resumida desta reportagem
Republicar
