A prolongada crise sanitária causada pela pandemia continua acelerando o desenvolvimento de novos tipos de vacinas. Depois de a Covid-19 ter sido alvo no final de 2020 das primeiras vacinas baseadas na ação do RNA mensageiro (mRNA) aprovadas para uso em humanos, um novo avanço significativo na área de imunizantes foi obtido em agosto deste ano: a farmacêutica indiana Zydus Cadila conseguiu aprovar de forma emergencial a primeira vacina de DNA diretamente injetado no corpo humano, também voltada para o combate do Sars-CoV-2. Essa tecnologia é estudada desde os anos 1990 e, até agora, era utilizada no campo veterinário. Existem pelo menos mais 10 candidatos a imunizantes contra a Covid-19 em testes que usam moléculas circulares de DNA, os chamados plasmídeos, como plataforma para desenvolver vacinas contra a doença.
A vacina indiana de DNA, denominada ZyCoV-D, será utilizada de forma emergencial entre os indianos. Ela deve ser administrada pela pele, com um dispositivo que não usa agulha e em três doses, com um intervalo de 28 dias entre as aplicações. O imunizante se destina a pessoas com mais de 12 anos. Seus testes de fase 3 estão sendo feitos com mais de 28 mil pessoas e os dados preliminares indicam uma proteção de 67% contra o aparecimento de casos sintomáticos da altamente transmissível variante delta do Sars-CoV-2, originária da Índia. Mesmo com eficácia inferior às vacinas de mRNA, o resultado é relevante. “Esse é um passo realmente importante na luta para derrotar a Covid-19 globalmente, porque demonstra que temos outra classe de vacinas para usar”, disse à revista Nature o imunologista pediátrico Peter Richmond, da Universidade da Austrália Ocidental em Perth, não envolvido no desenvolvimento do produto.
Segundo o imunologista Gustavo Cabral de Miranda, do Instituto de Ciências Biomédicas da Universidade de São Paulo (ICB-USP), as vacinas de DNA apresentam características interessantes. “Elas podem ser arquitetadas de forma a gerar uma resposta imunológica extremamente eficiente e completa, principalmente na ativação das células T [que compõem a resposta imunitária celular, tão importante no combate ao vírus quanto os anticorpos]”, afirma Miranda.
A aplicação da ZyCoV-D é feita por via intradérmica, sob as primeiras camadas da pele, em vez de ser administrada no tecido muscular
Em relação às vacinas de mRNA, como as da Moderna e da Pfizer/BioNTtech contra Covid-19, os imunizantes baseados em DNA apresentam, em tese, algumas vantagens: são mais fáceis e baratos de produzir e não precisam de condições especiais para serem armazenados, uma vantagem a favor do seu emprego em lugares remotos ou com pouca infraestrutura. Segundo a empresa indiana, a ZyCoV-D pode ser armazenada entre -2 °C e 8 °C, temperaturas similares à da maioria das vacinas contra outras doenças. Além disso, ela permanece estável por até três meses se mantida a 25 °C. “A aprovação dessa vacina de DNA para humanos representa um grande avanço científico que beneficia países que ainda têm dificuldade de acesso às vacinas por questões de transporte e estocagem”, diz o biotecnólogo brasileiro Gustavo Moreira, da Universidade Técnica de Braunschweig, na Alemanha, que estuda o desenvolvimento de vacinas. “Países como o Brasil podem ser altamente beneficiados se conseguirem nacionalizar a produção, uma vez que essa tecnologia é mais simples e facilmente adaptável caso novas variantes ou novos vírus surjam no futuro.”
O raciocínio por trás do funcionamento das vacinas de DNA é similar ao dos imunizantes de mRNA: colocar a maquinaria celular do hospedeiro em contato com as instruções genéticas necessárias para fabricar uma versão modificada e inócua, mas reconhecível, de uma proteína típica do patógeno infectante. Essa proteína é o antígeno contra o qual o sistema imunológico produzirá células de defesa específicas que vão defender o organismo quando entrar em contato de fato com o patógeno.
Nesse trabalho de levar a receita para fabricar o antígeno, as vacinas de DNA necessitam, para funcionar, de um passo a mais do que as de mRNA. Isso porque, uma vez dentro do organismo, as instruções genéticas contidas nos plasmídeos de DNA devem ser transcritas na forma da molécula de mRNA, que será decodificada nos ribossomos, “máquinas” de sintetizar proteínas. Os imunizantes à base de mRNA já entregam o receituário genético diretamente para a síntese do antígeno, pulando a etapa de codificar primeiramente a mensagem a partir do DNA.
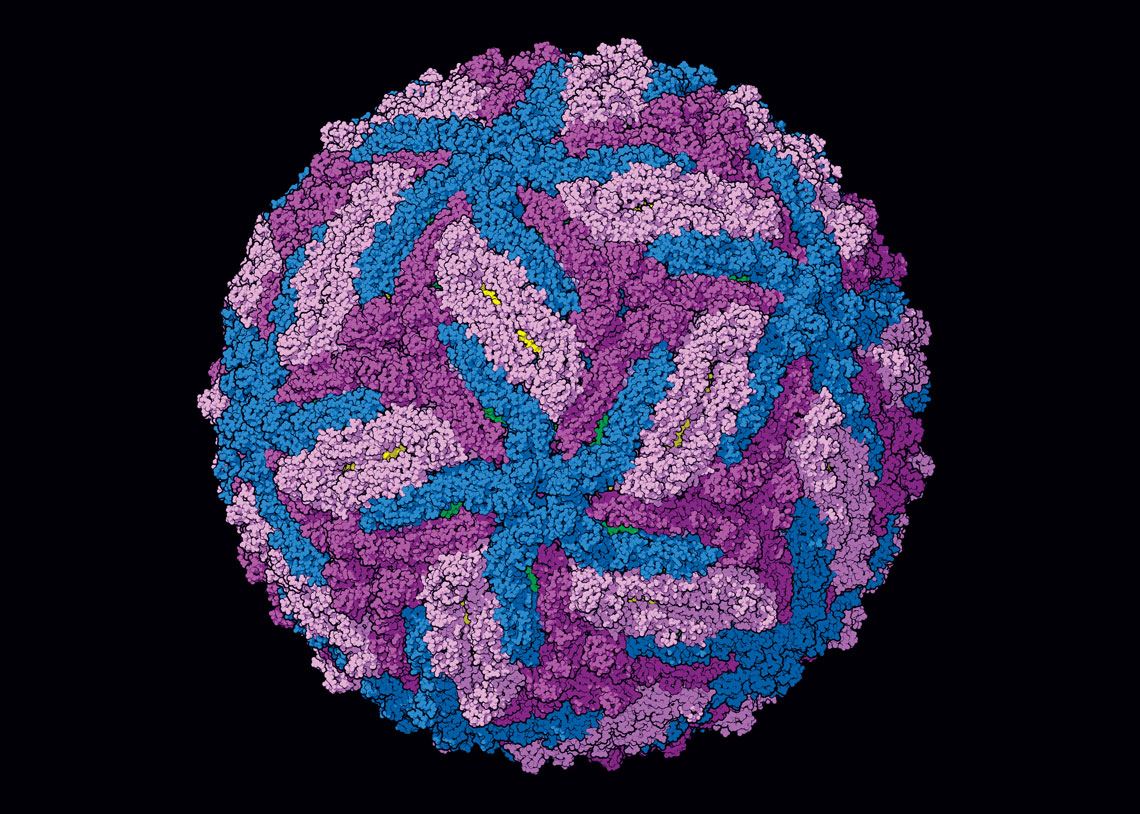
Manuel Almagro Rivas / Wikimedia Commons
A tecnologia de mRNA é uma das possibilidades para desenvolver imunizantes contra outros vírus além do Sars-CoV-2, como o da febre zika…Manuel Almagro Rivas / Wikimedia CommonsNo caso da ZyCoV-D, os plasmídeos conseguiram induzir com sucesso a produção de uma proteína de superfície do Sars-CoV-2, a spike, que forma as espículas responsáveis por ajudar o vírus a penetrar nas células humanas. A spike é o principal antígeno de todas as vacinas aprovadas contra Covid-19, independentemente da tecnologia empregada pelo imunizante. Uma vez no organismo, os plasmídeos geralmente se degradam em semanas ou, no máximo, em meses, mas a imunidade induzida permanece.
Apesar de apresentar algumas vantagens em relação às vacinas de mRNA, os imunizantes baseados na tecnologia do DNA enfrentam um obstáculo que foi contornado, ao menos parcialmente, pela ZyCoV-D. Elas têm de levar a informação genética dos plasmídeos diretamente ao núcleo das células das pessoas que recebem o imunizante. É no núcleo que está a enzima que copia o DNA para o RNA. Normalmente, o núcleo celular é de difícil acesso e baixas quantidades de plasmídeos conseguem alcançá-lo. No caso das vacinas de mRNA, as instruções para fabricar o antígeno precisam chegar apenas no citoplasma, espaço preenchido por um líquido que se situa entre o núcleo e a membrana plasmática (que marca os limites da célula). No citoplasma, ficam em suspensão as organelas celulares, como os ribossomos, responsáveis pela produção das proteínas a partir da receita entregue pelo mRNA.
Essa limitação das vacinas de DNA fez com que elas geralmente provocassem fracas respostas imunológicas nos ensaios clínicos. Por isso, até agora, só havia vacinas baseadas em plasmídeos aprovadas para uso em animais, como cavalos ou cachorros, para prevenir câncer de pele. Segundo a indiana Zydus Cadila, a baixa eficácia das vacinas de DNA foi superada com modificações na forma de administrar o novo imunizante contra a Covid-19.
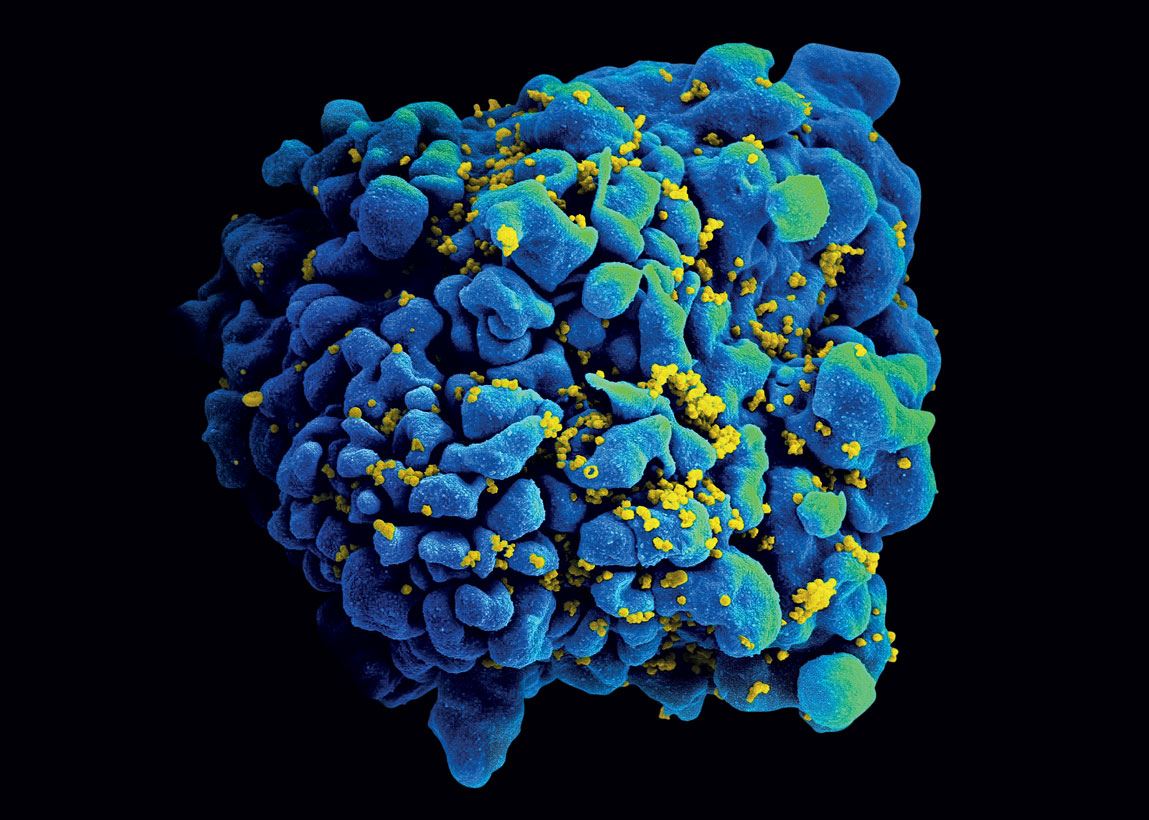
NIAID
e o HIV da Aids (ao lado, infectando células)NIAIDA aplicação da ZyCoV-D é feita por via intradérmica, sob as primeiras camadas da pele, em vez de ser administrada profundamente no tecido muscular, como na maioria das vacinas. O dispositivo usado pelos indianos não envolve perfurações. Ele deve ser simplesmente pressionado contra o corpo. Dessa forma, cria-se um fluxo fino de alta pressão que consegue atravessar as camadas celulares com o imunizante. Como a pele é rica em células imunológicas, ao contrário dos músculos, seria mais fácil para o organismo absorver e processar as partículas da vacina. “Essa forma de aplicação ajuda a capturar o DNA com muito mais eficiência do que no músculo”, afirmou à Nature o virologista indiano Shahid Jameel, da Universidade Ashoka, que não participou do desenvolvimento da vacina da Zydus Cadila. As três doses preconizadas do imunizante também são uma forma de tentar aumentar a eficácia do produto.
Na esteira do desenvolvimento da vacina de DNA indiana existem ao menos outras 10 sendo testadas no mundo, nenhuma no Brasil. Uma das principais diferenças entre elas é a forma de aplicação, conforme mostra a plataforma Clinical Trials. Além da região intradérmica, também se investiga se a via muscular pode ser a mais indicada para conseguir uma resposta imunológica potente. Entre as iniciativas que tentam solidificar uma forma mais rápida de atingir os núcleos celulares por meio da pele, a desenvolvida pela empresa de biotecnologia americana Inovio Pharmaceuticals apresenta uma importante diferença. Apesar de também usar um plasmídeo para codificar a proteína spike, a aplicação do imunizante por via intradérmica é realizada por meio de eletroporação, ou seja, pulsos elétricos curtos são aplicados na pele para aumentar a permeabilidade da membrana celular. Segundo os estudos pré-clínicos e de fase 1 (em que se mede a segurança e a tolerância do produto), o mecanismo não apenas aumentou a permeabilidade da membrana celular como melhorou a absorção do antígeno, deflagrando assim uma resposta imunológica mais eficaz. A eletroporação também foi associada a um aumento da resposta imune por meio do maior recrutamento de células inflamatórias no local da aplicação.
A pandemia mudou os planos científicos de muitos grupos de pesquisa que estudam vacinas e vírus pelo mundo e tem impulsionado o desenvolvimento de imunizantes não apenas contra o novo coronavírus. Outras doenças, para as quais não há vacinas, talvez possam ser mais bem enfrentadas daqui para frente com a experiência de controle da pandemia. A empresa Moderna, por exemplo, começou a testar recentemente em humanos duas novas vacinas contra o HIV, baseadas na tecnologia do RNA mensageiro. A expectativa da companhia é que os estudos apresentem os primeiros resultados em até um ano e meio. A busca por um imunizante contra a Aids tem sido inglória. No final de agosto, foi divulgado, por exemplo, que uma vacina contra o HIV que a Johnson & Johnson desenvolveu, com uma tecnologia parecida à usada em seu imunizante contra Covid-19, falhou em oferecer proteção segura a 2.600 mulheres que participaram de testes iniciais conduzidos no sul da África.
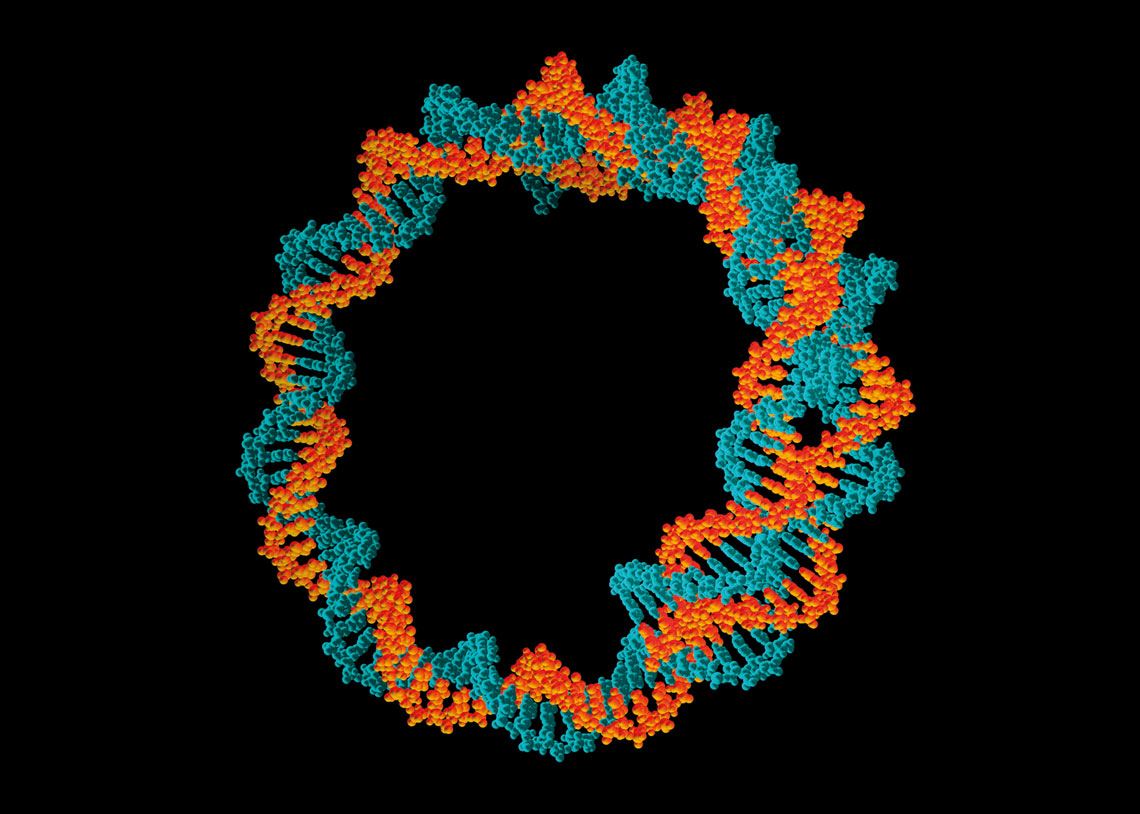
PASIEKA / SPL / Getty Images
A nova vacina indiana usa moléculas circulares de DNA, denominadas plasmídeos, para levar a informação genética para produzir a proteína spike do Sars-CoV-2PASIEKA / SPL / Getty ImagesUm dos benefícios proporcionados pelas tecnologias baseadas em mRNA e DNA é o curto espaço de tempo com que os ensaios clínicos podem ser montados a partir da concepção dos produtos. Existe até a possibilidade de testar diferentes variantes de antígenos na mesma vacina, uma estratégia que poderia ser útil na busca por imunizantes capazes de dar conta de mais de uma variante de um patógeno, como é o caso das distintas linhagens do Sars-CoV-2 em circulação no mundo.
Por ora, as pesquisas com vacinas de mRNA estão mais avançadas do que as de DNA. Além da Aids, imunizantes que adotam essa estratégia também estão sendo criados contra outras doenças, como zika, malária, gripe e até diferentes tipos de câncer. A alemã BioNTech, que desenvolveu a tecnologia de mRNA usada na vacina lançada em conjunto com a Pfizer, foi concebida para criar terapias personalizadas, em especial na área oncológica. Uma das dificuldades vencidas foi conferir estabilidade às formulações de imunizantes com mRNA. Isso foi conseguido quando se descobriu que revestir a molécula com uma capa de lipídios, um tipo de gordura, evitava sua degradação. Restou, no entanto, o inconveniente de ter de armazenar as vacinas de mRNA a temperaturas muito baixas.
Republicar
