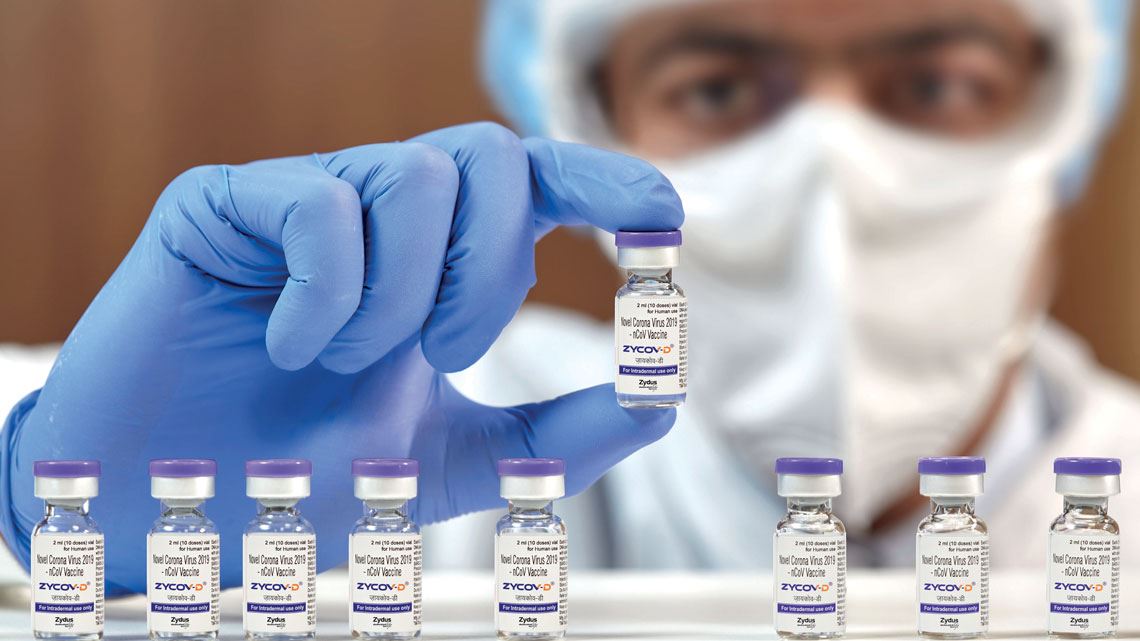
La prolongada crisis sanitaria causada por la pandemia continúa acelerando el desarrollo de nuevos tipos de vacunas. Luego de que el covid-19 fuera el blanco de las primeras vacunas basadas en la acción del ARN mensajero (ARNm) aprobadas para su uso en humanos, a finales de 2020, en agosto de este año se ha logrado un nuevo avance significativo en el área de los inmunógenos: la empresa farmacéutica india Zydus Cadila obtuvo la aprobación en carácter de emergencia de la primera vacuna de ADN para su inoculación directa en el cuerpo humano, también centrada en la lucha contra el Sars-CoV-2. Esta tecnología se venía estudiando desde la década 1990 y, hasta ahora, se utilizaba en el campo veterinario. Se encuentran en fase de prueba al menos otros 10 posibles inmunizantes contra el covid-19 que utilizan moléculas circulares de ADN, los denominados plásmidos, como plataforma para el desarrollo de vacunas contra la enfermedad.
La vacuna india de ADN, denominada ZyCoV-D, se utilizará bajo el formato de emergencia en la población india. Se administrará a través de la piel, mediante un dispositivo que no requiere aguja y constará de tres dosis, que se aplicarán con un intervalo de 28 días. El inmunógeno está destinado a las personas mayores de 12 años. Se están llevando a cabo los ensayos clínicos de la fase III con más de 28.000 voluntarios y los datos preliminares indican una protección de un 67 % contra la aparición de casos sintomáticos de la altamente transmisible variante delta del Sars-CoV-2, originaria de la India. Estos resultados son relevantes, aunque su eficacia es inferior a la de las vacunas de ARNm. “Es un avance realmente importante en la lucha para derrotar al covid-19 en todo el mundo, pues demuestra que contamos también con otra clase de vacunas”, le dijo a la revista Nature el inmunólogo pediátrico Peter Richmond, de la Universidad de Australia Occidental en Perth, quien no participó en el desarrollo del producto.
Según el inmunólogo Gustavo Cabral de Miranda, del Instituto de Ciencias Biomédicas de la Universidad de São Paulo (ICB-USP), las vacunas de ADN presentan características interesantes. “Se las puede diseñar para generar una respuesta inmunológica extremadamente eficiente y completa, principalmente en cuanto a la activación de las células T [que forman parte de la respuesta inmunitaria celular, tan importante para combatir al virus como los anticuerpos]”, dice Cabral de Miranda.
La aplicación de la Zycov-D se realiza por vía intradérmica, bajo las primeras capas de la piel, en lugar de inoculársela en el tejido muscular
En comparación con las vacunas de ARNm, como en los casos de los inmunógenos contra el covid-19 de Moderna y Pfizer/BioNTech, las que están basadas en ADN ofrecen, en teoría, algunas ventajas: son más fáciles y baratas de producir y no requieren condiciones especiales para su conservación, un punto a favor para su empleo en lugares remotos o con escasa infraestructura. Según informa la empresa india, la ZyCoV-D puede almacenarse en un rango entre -2 ºC y 8 ºC, temperaturas similares a las de la mayoría de las vacunas contra otras enfermedades. Además, se conserva estable hasta tres meses si se la mantiene a 25 ºC. “La aprobación de esta vacuna de ADN de uso humano representa un gran avance científico que beneficia a países que aún enfrentan dificultades para acceder a las vacunas debido a cuestiones de transporte y almacenamiento”, dice el biotecnólogo brasileño Gustavo Moreira, de la Universidad Técnica de Brunswick, en Alemania, quien estudia el desarrollo de inmunógenos. “Países como Brasil podrían en gran medida beneficiarse si consiguen nacionalizar la producción, puesto que esta tecnología es más sencilla y fácilmente adaptable si en el futuro surgen nuevas variantes o virus nuevos”.
El razonamiento en el cual se basa el funcionamiento de las vacunas de ADN es similar al de los agentes inmunizantes de ARNm: poner en contacto a la maquinaria celular del hospedante con las instrucciones genéticas necesarias para elaborar una versión modificada e inocua, pero reconocible, de una proteína típica del patógeno infeccioso. Esta proteína es el antígeno contra el cual el sistema inmunológico producirá las células de defensa específicas que resguardarán al organismo cuando entable un contacto real con el patógeno.
En esta tarea de incorporar la receta para fabricar el antígeno, las vacunas de ADN necesitan, para poder funcionar, un paso más que las de ARNm. Sucede que, una vez dentro del organismo, las instrucciones genéticas presentes en los plásmidos de ADN deben transcribirse en el formato de molécula de ARNm, que será decodificada en los ribosomas, las “máquinas” que sintetizan las proteínas. Las vacunas diseñadas con base en ARNm ya entregan la receta genética directamente para la síntesis del antígeno, salteándose la etapa de codificar previamente el mensaje a partir del ADN.

Manuel Almagro Rivas / Wikimedia Commons
La tecnología de ARNm es una de las posibilidades para el desarrollo de vacunas contra otros virus, además del Sars-CoV-2, tales como el de la fiebre del Zika…Manuel Almagro Rivas / Wikimedia CommonsEn el caso de la ZyCoV-D, los plásmidos indujeron exitosamente la producción de una proteína de superficie del Sars-CoV-2, la spike, que forma las espículas de las cuales se vale el virus para penetrar en las células humanas. La spike es el antígeno principal de todas las vacunas aprobadas contra el covid-19, independientemente de la tecnología empleada por cada una. Una vez en el organismo, los plásmidos normalmente se degradan al cabo de unas semanas o, como máximo, unos meses, pero la inmunidad inducida permanece.
Pese a que ofrecen algunas ventajas en comparación con las vacunas de ARNm, los inmunógenos basados en la tecnología de ADN se enfrentan a un obstáculo que ha podido esquivar, al menos parcialmente, la ZyCoV-D. Deben llevar la información genética de los plásmidos directamente al núcleo de las células del individuo inoculado. Es en el núcleo donde se encuentra la enzima que transcribe el ADN en ARN. Normalmente, el acceso al núcleo celular es difícil y son pocos los plásmidos que logran alcanzarlo. En el caso de las vacunas de ARNm, las instrucciones para fabricar el antígeno solamente necesitan llegar al citoplasma, un espacio ocupado por un líquido entre el núcleo y la membrana plasmática (que marca los límites de la célula). En el citoplasma, se encuentran en suspensión orgánulos celulares como los ribosomas, responsables de la producción de proteínas a partir de la receta entregada por el ARNm.
Esta limitación de las vacunas de ADN ha hecho que, por lo general, susciten una respuesta inmunológica débil en los ensayos clínicos. Por eso, hasta ahora, solo había vacunas basadas en plásmidos aprobadas para su uso en animales, tales como caballos o perros, para prevenir el cáncer de piel. Según informa la empresa india Zydus Cadila, la baja eficacia de las vacunas de ADN ha podido superarse modificando la forma de administrar el nuevo inmunógeno contra el covid-19.
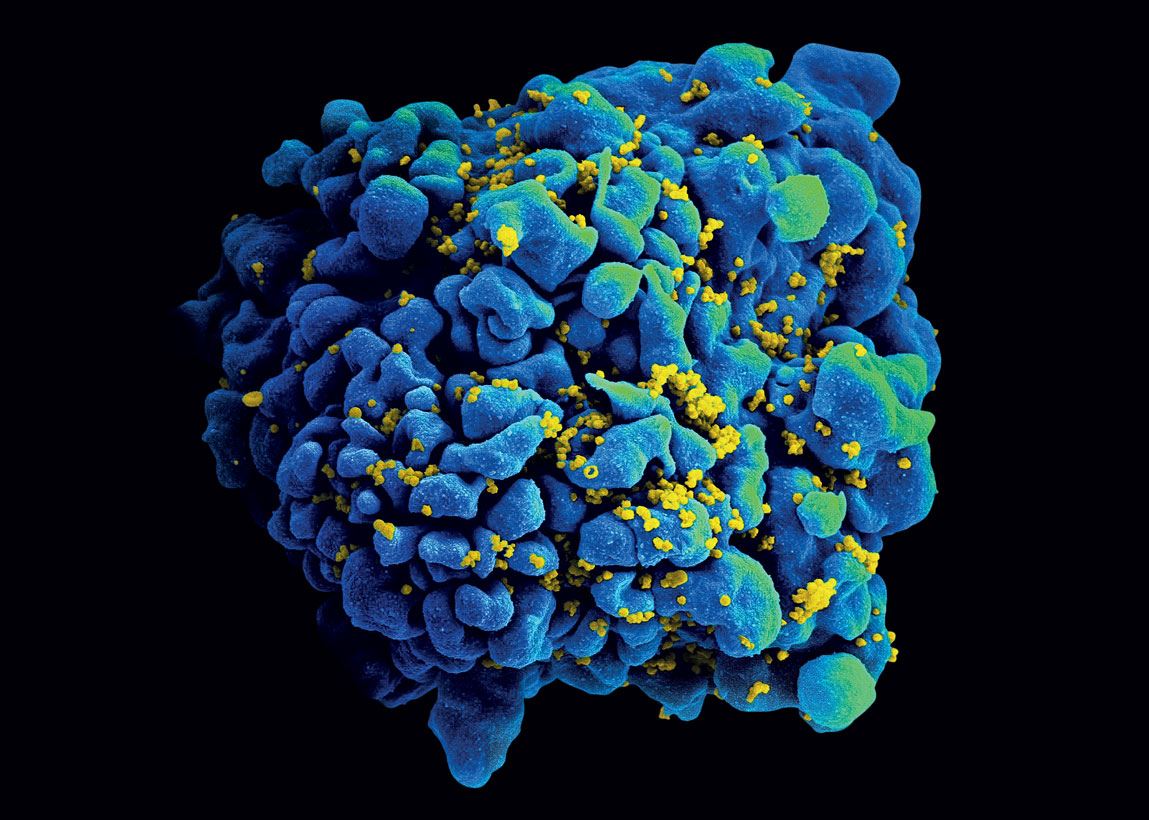
NIAID
…y el VIH del sida (infectando células)NIAIDLa ZyCoV-D se aplica por vía intradérmica, bajo las primeras capas de la piel, en lugar de administrarse en el tejido muscular profundo, como la mayoría de las vacunas. El dispositivo que utilizan los indios no implica pinchazos. Simplemente se presiona contra el cuerpo. De esta forma se genera una fina corriente de alta presión que logra atravesar las capas celulares introduciendo consigo el agente inmunizante. Como en la piel abundan las células inmunitarias, al contrario que en los músculos, al organismo le resultaría más fácil absorber y procesar las partículas de la vacuna. “Este método de aplicación ayuda a capturar el ADN de manera mucho más eficiente que el tejido muscular”, le aseguró a Nature el virólogo indio Shahid Jameel, de la Universidad Ashoka, quien no tuvo participación el desarrollo de la vacuna de Zydus Cadila. Las tres dosis recomendadas del agente inmunizante también tienen el objetivo de tratar de aumentar la eficacia del producto.
En la senda del desarrollo de la vacuna india de ADN, en todo el mundo hay al menos otras 10 similares en fase de prueba, ninguna de ellas en Brasil. Una de las diferencias principales entre ellas es la forma de aplicación, según consta en la plataforma Clinical Trials. Además de la zona intradérmica, también se está investigando si la vía muscular podría ser la más apropiada para conseguir una respuesta inmunológica potente. Entre las propuestas que procuran consolidar una forma más rápida de llegar a los núcleos celulares a través de la piel, la que ha desarrollado la empresa de biotecnología estadounidense Inovio Pharmaceuticals presenta una diferencia significativa. Aunque también utiliza un plásmido para codificar la proteína spike, la aplicación del inmunógeno por vía intradérmica tiene lugar mediante la técnica de electroporación, que consiste en la aplicación de breves pulsos eléctricos en la piel para aumentar la permeabilidad de la membrana celular. Según los resultados de los estudios preclínicos y de la fase I (que miden la seguridad y la tolerancia del producto), el mecanismo no solo incrementó la permeabilidad de la membrana celular, sino que mejoró la absorción del antígeno, desencadenando así una respuesta inmunitaria más eficaz. La electroporación también ha sido asociada a un aumento de la respuesta inmune merced a un mayor reclutamiento de células inflamatorias en la zona de aplicación.
La pandemia ha modificado los planes científicos de muchos grupos de investigación que estudian vacunas y virus en todo el mundo y ha impulsado el desarrollo de inmunógenos no solo contra el nuevo coronavirus. De aquí en adelante, a partir de la experiencia de control de la pandemia, tal vez sea posible hacer frente de mejor manera a otras enfermedades para las cuales no existen vacunas. La empresa Moderna, por ejemplo, ha comenzado recientemente a probar en humanos dos nuevas vacunas contra el VIH, basadas en la tecnología del ARN mensajero. La compañía espera tener los primeros resultados de los estudios de aquí a un año y medio. Hasta ahora, la búsqueda de una vacuna contra el sida ha sido infructuosa. A finales de agosto, se dio a conocer, por ejemplo, que una vacuna contra el VIH desarrollada por la compañía Johnson & Johnson con una tecnología similar a la utilizada en su agente inmunizante contra el covid-19, defeccionó al tratar de ofrecer una protección segura a 2.600 mujeres que participaron en los ensayos iniciales que se llevaron a cabo en el sur de África.
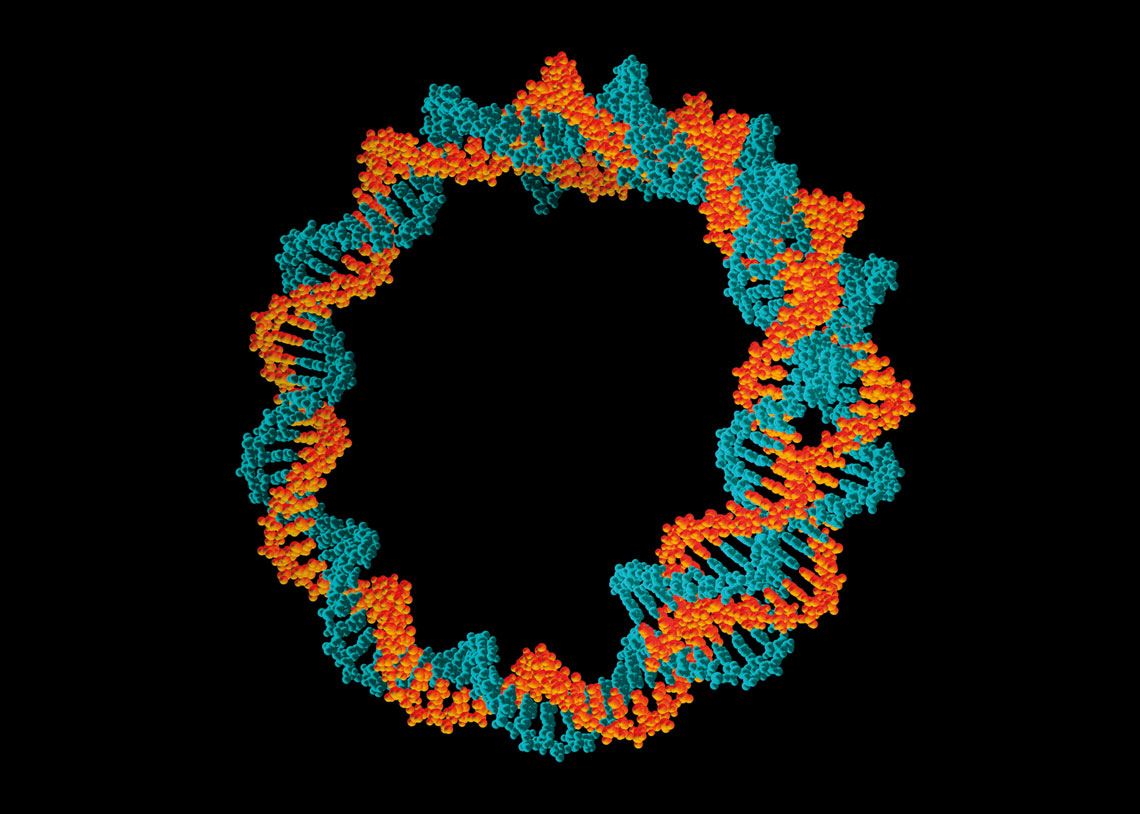
Pasieka / SPL / Getty Images
La nueva vacuna india utiliza moléculas circulares de ADN, denominadas plásmidos, para llevar la información genética para producir la proteína spike del Sars-CoV-2Pasieka / SPL / Getty ImagesUno de los beneficios que aportan las tecnologías basadas en ARNm y ADN es el breve espacio de tiempo en que pueden ejecutarse los ensayos clínicos a partir de la concepción de los productos. Incluso existe la posibilidad de testear diferentes variantes de antígenos en una misma vacuna, una estrategia que podría ser útil en la búsqueda de agentes inmunizantes capaces de proteger contra más de una variante de un patógeno, como en el caso de los distintos linajes del Sars-CoV-2 que circulan en el mundo.
Por el momento, las investigaciones con las vacunas de ARNm están más avanzadas que las de ADN. Además del sida, también están en desarrollo vacunas que adoptan esta misma estrategia contra otras enfermedades, tales como el zika, el paludismo, la gripe e incluso diversos tipos de cáncer. La firma alemana BioNTech, que desarrolló la tecnología de ARNm que se utiliza en la vacuna lanzada conjuntamente con Pfizer, la concibió para crear terapias personalizadas, especialmente en el campo de la oncología. Una de las dificultades superadas consistió en conferirle estabilidad a las fórmulas de inmunógenos con ARNm. Esto se consiguió cuando se descubrió que al revestir la molécula con una capa de lípidos –un tipo de grasas– se evitaba su degradación. Sin embargo, no pudo superarse el inconveniente de tener que almacenar estas vacunas a temperaturas muy bajas.
Republicar