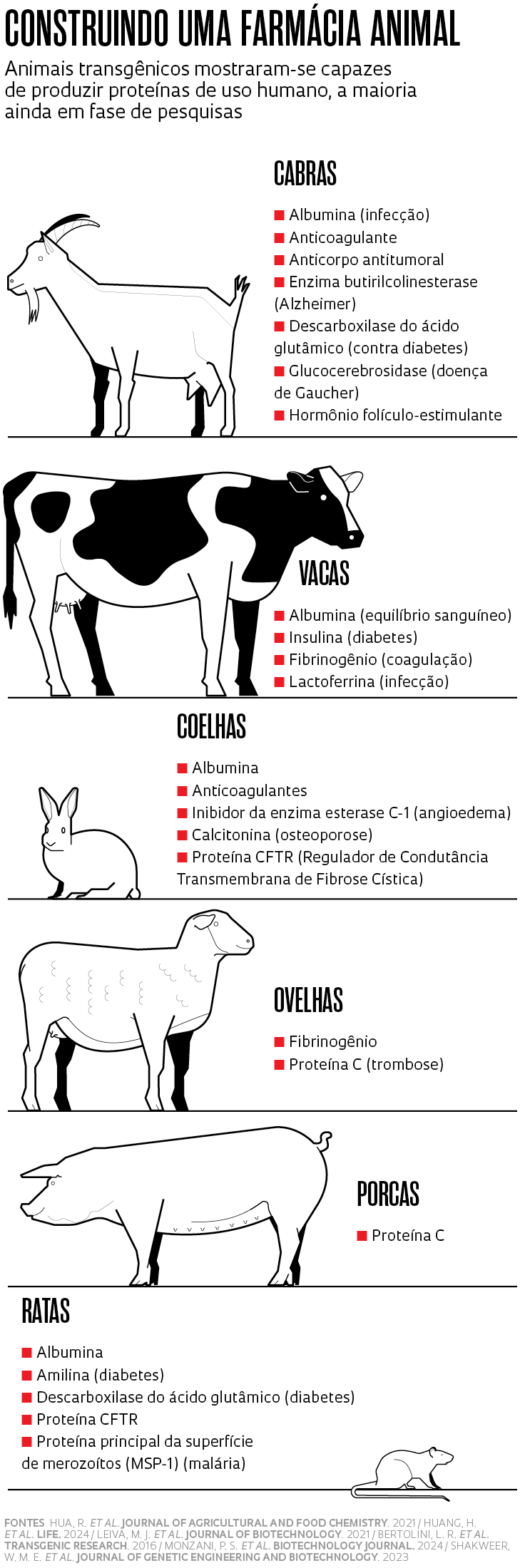
Em um artigo científico publicado em março deste ano na revista Biotechnology Journal, pesquisadores das universidades de São Paulo (USP), do Norte do Paraná (Unopar) e de Illinois, nos Estados Unidos, mostraram que uma vaca transgênica que eles desenvolveram havia produzido leite contendo insulina humana. O hormônio controla os níveis de glicose no sangue, essencial para quem tem diabetes. O trabalho, uma prova de conceito, não prosseguiu, mas alimenta a possibilidade, já indicada por outros grupos de pesquisa, de produzir medicamentos de uso humano na glândula mamária de vacas, cabras e coelhas modificadas geneticamente (ver infográfico mais abaixo).
Ainda não há fármacos desse tipo produzidos no Brasil. No exterior, a Agência de Medicamentos da Europa (EMA) e a Food and Drug Administration (FDA), órgão que regula alimentos e remédios nos Estados Unidos, aprovaram em 2006 e 2009, respectivamente, o primeiro medicamento do gênero, uma antitrombina humana recombinante. Produzida em leite de cabras transgênicas pela farmacêutica norte-americana LFB Biotechnology, ela é indicada para pessoas com deficiência hereditária da proteína antitrombina. Essa molécula inibe a coagulação do sangue e reduz o risco de obstrução dos vasos sanguíneos e de infarto.
Outra proteína recombinante humana, extraída do leite de coelhas transgênicas, foi aprovada para venda na Europa em 2012 e nos Estados Unidos em 2014. Produzido pela empresa holandesa Pharming Group e pela norte-americana Salix Pharmaceutics, o medicamento é indicado para a forma hereditária de angioedema, doença rara causada pela deficiência na produção de uma proteína do sangue chamada inibidor da enzima esterase C1.
Mais recentemente, em 2020, a FDA aprovou uma proteína, também da LFB, que ajuda a coagulação sanguínea. Ela é produzida em glândulas mamárias de coelhas transgênicas. Além desses três medicamentos já lançados no mercado, várias outras proteínas de uso humano foram produzidas experimentalmente em animais, inclusive no Brasil.
A história do leite transgênico brasileiro contendo insulina humana começou em 2008, na Faculdade de Zootecnia e Engenharia de Alimentos (FZEA) da USP, campus de Pirassununga. Lá, o veterinário Flávio Meirelles e o biólogo Paulo Monzani começaram a preparar um tipo de cromossomo artificial (plasmídeo) utilizando o gene que poderia ativar, inicialmente, a produção do fator IX de coagulação humana. O plasmídeo foi colocado em um vírus, que se incorporou ao DNA de um fibroblasto, tipo de célula que aceita materiais estranhos com relativa facilidade. O fibroblasto modificado geneticamente se fundiu com uma célula reprodutiva feminina, chamada de ovócito, sem núcleo, e o embrião que começou a se formar foi então transferido para o útero de uma vaca. Em 1996, um processo semelhante gerou a ovelha Dolly, o primeiro animal clonado a partir de uma célula adulta de outra ovelha.
Duas bezerras geneticamente modificadas para o fator IX de coagulação humana nasceram em 2010, mas morreram logo depois. Em seguida, Meirelles e Monzani começaram a trabalhar com o grupo do veterinário Otavio Mitio Ohashi, da Unopar, para produzir vacas transgênicas capazes de formular fármacos como a insulina humana. Na Unopar, Monzani construiu outros plasmídeos, entre eles os da insulina, incorporados por fibroblastos de uma vaca da raça jersey.
“Diversas transferências de embrião não vingaram”, conta Meirelles. “A clonagem tem baixa eficiência.” Após várias tentativas, uma vaca com o gene da pró-insulina humana nasceu em 2014 e cresceu em uma fazenda do interior do Paraná, do proprietário da Unopar, Marco Laffranchi (1936-2015). Como não engravidava, mesmo após se tentar diferentes técnicas reprodutivas, o animal passou por uma indução hormonal da lactação e produziu leite com insulina humana. Um imprevisto, entretanto, interrompeu a pesquisa: “A vaca morreu no pasto, possivelmente picada por uma cobra, em 2022”, lamenta Monzani.
Sem financiamento, a investigação parou, mas Meirelles continua convencido de que as glândulas mamárias de vacas, cabras e outros animais de criação podem ser um ótimo ambiente – ou biorreator, na linguagem mais formal – para a produção de medicamentos de uso humano: “A proporção de proteínas transgênicas no leite é da ordem de gramas por litro, um rendimento muito maior do que o das técnicas convencionais”.
Pesquisas interrompidas são comuns nesse campo. Um grupo da empresa argentina Biosidus anunciou em 2007 o nascimento de quatro vacas da raça jersey capazes de produzir leite com insulina humana (ver Pesquisa FAPESP nº 147). Na época, comentou-se que bastariam 25 vacas para abastecer toda a demanda dos argentinos por insulina, que poderia ter um preço pelo menos 30% menor que a produzida por outras técnicas. Passados 17 anos, não há mais notícias sobre esse programa da empresa – a reportagem de Pesquisa FAPESP tentou contato com os responsáveis, que não se manifestaram.
O que se sabe vem de um relatório sobre biotecnologia agrícola na Argentina publicado em dezembro de 2022 pelo Departamento de Agricultura dos Estados Unidos. “Embora existam regulamentações para a aprovação de animais geneticamente modificados, não há produção comercial na Argentina, nem para fins agrícolas, nem para pesquisa biomédica, produção farmacêutica ou produção de órgãos para transplante”, informa o documento. Ainda de acordo com o relatório, o interesse dos produtores por animais transgênicos diminuiu nos últimos anos, à medida que a legislação europeia proibia a importação de animais ou produtos transgênicos.
Experimentalmente, o leite de vacas transgênicas serviu também para produzir hormônio de crescimento humano, albumina, anticorpo monoclonal contra câncer e proteínas que facilitam a coagulação sanguínea. Em geral, os relatos, como os do grupo da USP, não informam o rendimento obtido, mas em 2014 pesquisadores da Universidade de Vermont, nos Estados Unidos, utilizando camundongos fêmeas transgênicas, obtiveram 8,1 gramas por litro (g/L) de insulina humana.
Desde os anos 1980, esse hormônio, fundamental para o controle do diabetes, é produzido por meio do cultivo de bactérias Escherichia coli geneticamente modificadas. Uma das poucas empresas no mundo que dominavam a técnica de produção de insulina por E. coli era a Biobrás, criada por pesquisadores da Universidade Federal de Minas Gerais (UFMG). Em 2001, ela foi comprada pela dinamarquesa Novo Nordisk e depois desativada. Os ex-diretores da Biobrás criaram a Biomm, que importa insulina (ver Pesquisa FAPESP nº 302). Atualmente, toda insulina consumida no Brasil é importada.

Paulo S. Morzani
A vaca da USP e UNOPAR cujo leite continha insulina humana
Paulo S. MorzaniPor E. coli, o rendimento é de 0,009 g por litro de meio de cultura, de acordo com uma análise das técnicas de produção de insulina por microrganismos publicada em outubro de 2014 na revista Microbial Cell Factories. Outra comparação, na revista Transgenic Research de junho de 2016, observa que a mesma quantidade de proteína recombinante obtida do leite de animais de criação custaria oito vezes menos que por cultura de células de ovário de hamster chinês, a fonte da proteína desejada.
“Ainda que tenham bons resultados iniciais, muitos projetos param porque são demorados e caros”, reconhece a veterinária Maria Angélica Miglino, da Universidade de Marília (Unimar), no interior paulista. Ela não participou do projeto da USP, mas há cerca de um ano ganhou de Monzani uma amostra de células epiteliais de glândula mamária de vaca. Seu propósito é construir, em laboratório, uma glândula mamária artificial, apta tanto a produzir leite quanto a servir de modelo experimental para estudo de doenças animais e humanas. Esse trabalho faz parte do doutorado do veterinário moçambicano Fernando Chissico na Unimar, sob sua orientação.
“O grande problema das proteínas recombinantes produzidas pela glândula mamária de animais não é a tecnologia, mas a regulamentação”, comenta a bióloga brasileira Luciana Relly, diretora científica da C&L Biotech, uma empresa de consultoria de animais transgênicos nos Estados Unidos. “Um fármaco produzido por animais transgênicos também tem de cumprir todas as etapas de testes pré-clínicos e clínicos e, além disso, atender às exigências de produção, assegurando que os animais e as proteínas recombinantes estejam livres de qualquer contaminação.”
De 2006 a 2015, na Universidade de Fortaleza (Unifor), no Ceará, ela foi uma das coordenadoras da pesquisa que culminou com o nascimento de uma cabra transgênica capaz de produzir leite com a enzima glucocerebrosidase, cuja deficiência causa a doença de Gaucher (ver Pesquisa FAPESP nº 236). Apesar de ter sido bastante noticiado e comemorado, o trabalho não avançou. “O governo federal preferiu negociar a transferência de tecnologia de produção de uma empresa de Israel, mas não avançou”, relata. Sem financiamento, o grupo da Unifor se desfez.
Relly transferiu-se para a Pontifícia Universidade Católica do Rio Grande do Sul (PUC-RS) em 2015. Cinco anos depois mudou-se para os Estados Unidos. A jornada a levou também a esta conclusão: “As glândulas mamárias são um excelente biorreator, principalmente para proteínas que não poderiam ser produzidas de outro modo, como o Atryn [nome comercial da antitrombina recombinante da LFB], difícil de fazer em células”.
Com o que aprenderam durante essa experiência, os pesquisadores que continuaram na Unifor, ex-alunos de pós-graduação dos coordenadores iniciais, ajudaram colegas da Universidade de Concepción, no Chile, a obter, a partir de leite de cabras, um anticorpo antitumoral, chamado de inibidor do fator de crescimento vascular endotelial (VEGF). Descrito em 2021 na revista científica Journal of Biotechnology, o processo reforça a possibilidade de implantar outras formas de produzir medicamentos de uso humano.
Fios de seda produzidos por cabras Leve, flexível e resistente, material poderia ser usado na fabricação de uniformes militares e cordas de raquetesGlândulas mamárias de animais transgênicos não têm sido investigadas apenas para produção de fármacos. Em 2002, o leite de cabra serviu como ambiente para a fabricação de fios de seda, depois de pesquisadores da empresa canadense Nexia Biotechnologies implantarem no animal genes de aranha capazes de produzi-los. Também chamado de bioaço, esse material interessa por ser leve, flexível e mais resistente que os fios de aço, com aplicações potenciais em uniformes militares, suturas (costuras) cirúrgicas ou cordas de raquetes de tênis.
A empresa faliu em 2009, mas o biólogo molecular Randy Lewis, da Universidade de Wyoming, nos Estados Unidos, continuou o trabalho e obteve 30 cabras transgênicas, mantidas em uma fazenda da Universidade Estadual de Utah, também nos Estados Unidos. De acordo com um comunicado da Universidade de Wyoming de outubro de 2023, apenas três de cada sete crias das cabras transgênicas possuem o gene da proteína. Sua experiência motivou a artista e empreendedora holandesa Jalila Essaïdi a criar, em 2011, uma empresa com o propósito de produzir roupas à prova de balas com fios de cabras transgênicas. Por enquanto, não há ainda um produto comercial.
A reportagem acima foi publicada com o título “Fármacos do leite transgênico” na edição impressa nº 339, de maio de 2024.
Projeto
Produção de embriões bovinos transgênicos para o fator IX de coagulação (nº 08/00102-0); Modalidade Bolsas no Brasil – Pós-doutorado; Pesquisador responsável Flávio Vieira Meirelles (USP); Beneficiário Paulo Sérgio Monzani; Investimento R$ 126.819,24.
Artigos científicos
BAESHEN, N. A. et al. Cell factories for insulin production. Microbial Cell Factories. v. 13, n. 141. 2 out. 2014.
BERTOLINI, L. R. et al. The transgenic animal platform for biopharmaceutical production. Transgenic Research. v. 25, p. 329-43. 28 jan. 2016.
Republicar