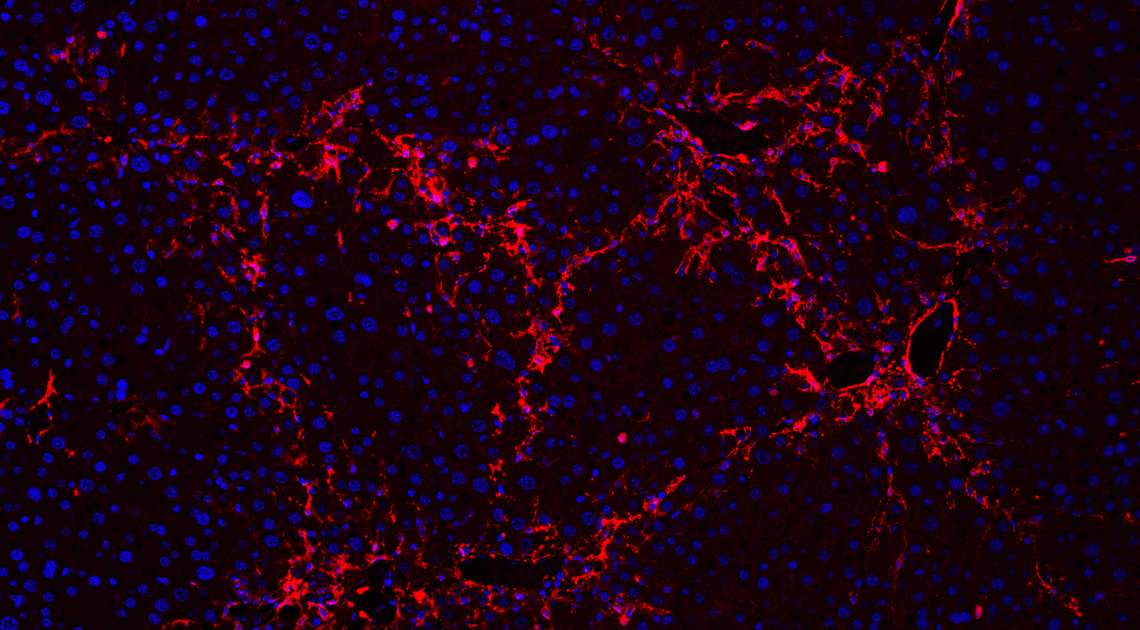
Em experimentos com camundongos, um grupo internacional de pesquisadores do qual participou o veterinário brasileiro Bruno Cogliati mostrou ser possível reprogramar células de defesa dos animais para combater um dos problemas hepáticos mais comuns em seres humanos: a fibrose decorrente do acúmulo de gordura no fígado, para a qual ainda são escassos os tratamentos disponíveis. Comum em pessoas com excesso de peso, diabetes ou desequilíbrio dos níveis de colesterol e outras gorduras no sangue, o acúmulo de gordura no fígado atinge de 30% a 40% da população adulta (os números variam segundo a região do mundo). De 4% a 8% delas desenvolvem fibrose mais intensa, com a formação de cicatrizes no órgão, que, a partir de certo estágio, se torna rígido e deixa de funcionar adequadamente – a forma mais avançada dessa fibrose, conhecida como cirrose, é uma importante causa de transplante de fígado. Uma das novidades do estudo, publicado no final de janeiro na revista Science Translational Medicine, é que a reprogramação das células de defesa ocorreu no próprio organismo dos roedores – in vivo, como dizem os pesquisadores –, sem a necessidade de extraí-las e manipulá-las em laboratório.
“Os resultados são animadores”, relata Cogliati, da Faculdade de Medicina Veterinária e Zootecnia da Universidade de São Paulo (FMVZ-USP), que colaborou nos experimentos durante o período sabático que, com apoio da FAPESP, iniciou em 2022 no grupo do hepatologista norte-americano Scott Friedman, da Escola de Medicina Icahn, no Hospital Mount Sinai, em Nova York. “Apesar do sucesso inicial, ainda precisamos de mais experimentos para conhecer quais seriam a dosagem adequada e o número de aplicações necessário para tratar diferentes graus de fibrose, antes de se pensar em testes com seres humanos”, explica o pesquisador, que permanecerá mais algum tempo no Mount Sinai.
Especialista em fibrose hepática, Cogliati investiga como o acúmulo de gordura altera a comunicação entre os diferentes tipos de células do fígado e leva ao surgimento de cicatrizes no órgão, que, com o tempo e o aumento da gravidade, pode resultar em falência (cirrose) ou originar um câncer. Há três anos, ele foi para o laboratório de Friedman interessado em detalhar o comportamento das células estreladas, que, em situações específicas, desencadeiam a fibrose.
No fígado sadio, as células estreladas desempenham várias funções benéficas, como demonstrou Cogliati em um artigo publicado em 2023 na revista Nature Reviews Gastroenterology & Pathology. Elas armazenam a vitamina A, essencial para a visão, e colaboram para a renovação celular em diferentes tecidos do corpo. Também auxiliam na manutenção e na proliferação dos hepatócitos, as células mais abundantes do fígado, responsáveis por produzir e armazenar proteínas, transformar carboidratos em reservas de energia, sintetizar colesterol e quebrar compostos tóxicos para o organismo.
Sob condições de dano ou estresse prolongado, como o causado por certas infecções ou quadros inflamatórios, porém, as células estreladas sofrem uma transformação radical: saem do estado de repouso ou quiescente, no qual realizam as funções metabólicas benéficas aos hepatócitos, e se tornam ativadas. Elas perdem seus depósitos de vitamina A, deixam de fornecer suporte aos hepatócitos, mudam de forma e passam a proliferar e migrar. Também iniciam a produção e a secreção de colágeno e de outras proteínas que formam uma rede de fibras no espaço entre as células – o acúmulo dessas fibras é chamado de fibrose ou cicatrização tecidual.
É o que acontece, por exemplo, com quem está com peso um tanto acima do ideal. Em excesso no organismo, a gordura passa a se acumular no interior dos hepatócitos e dispara uma inflamação. Células de defesa atacam os hepatócitos repletos de gordura e os matam, emitindo sinais químicos para as células estreladas. Estas, por sua vez, se tornam ativadas e iniciam a síntese e a liberação das fibras de colágeno e proteínas, que formam uma barreira ao redor das células eliminadas. Quanto maior o acúmulo de gordura no fígado, maior a extensão das cicatrizes, que, a partir do segundo dos quatro estágios de evolução, começam a prejudicar o funcionamento do órgão.
“Após certo grau de fibrose, o fígado reduz a produção de proteínas que levam nutrientes a outros tecidos, e o sangue passa a enfrentar resistência para irrigar o órgão. Essa resistência, ao se agravar, leva ao extravasamento de líquidos para a cavidade abdominal”, explica a hepatologista Claudia Souza de Oliveira, da Faculdade de Medicina da USP, que orientou Cogliati em um estágio de pós-doutorado e não participou da pesquisa atual. “Com o aumento da deposição de colágeno e o avanço da fibrose, os hepatócitos também deixam de produzir e excretar a bilirrubina, que se acumula nos tecidos e dá o tom amarelado à pele; de produzir fatores de coagulação, favorecendo a ocorrência de sangramentos; e de degradar substâncias tóxicas como a amônia, cujo aumento atrapalha o funcionamento cerebral”, conclui Oliveira.
No laboratório de Friedman no Mount Sinai, os pesquisadores decidiram buscar um modo de impedir – ou ao menos de reduzir – a cicatrização eliminando as células estreladas ativadas. Essas células, o grupo havia constatado, apresentam uma característica que as distingue das demais. Uma vez ativadas, passam a exibir em sua superfície uma quantidade abundante da proteína alfa de ativação dos fibroblastos (FAP). Essas proteínas seriam um alvo interessante para o qual direcionar as defesas do corpo e, assim, atingir apenas as células estreladas ativadas. O desafio era ensinar as células de defesa a reconhecer as FAP.
Uma forma de encaminhar os componentes do sistema imune para atingir um alvo celular específico é por meio da modificação de linfócitos T, uma família de células especializadas em identificar e destruir células doentes ou infectadas por patógenos. Para isso, os pesquisadores costumam extrair esses linfócitos do organismo e, em laboratório, alterá-los geneticamente para exibir em sua superfície um receptor quimérico de antígeno (CAR), uma espécie de ímã com predileção pelo alvo. Essa é a forma mais comum de produzir os chamados linfócitos ou células CAR-T. É uma estratégia complexa, trabalhosa e cara que vem sendo usada, por exemplo, para combater algumas formas de câncer (ver Pesquisa FAPESP nºs 286 e 354).
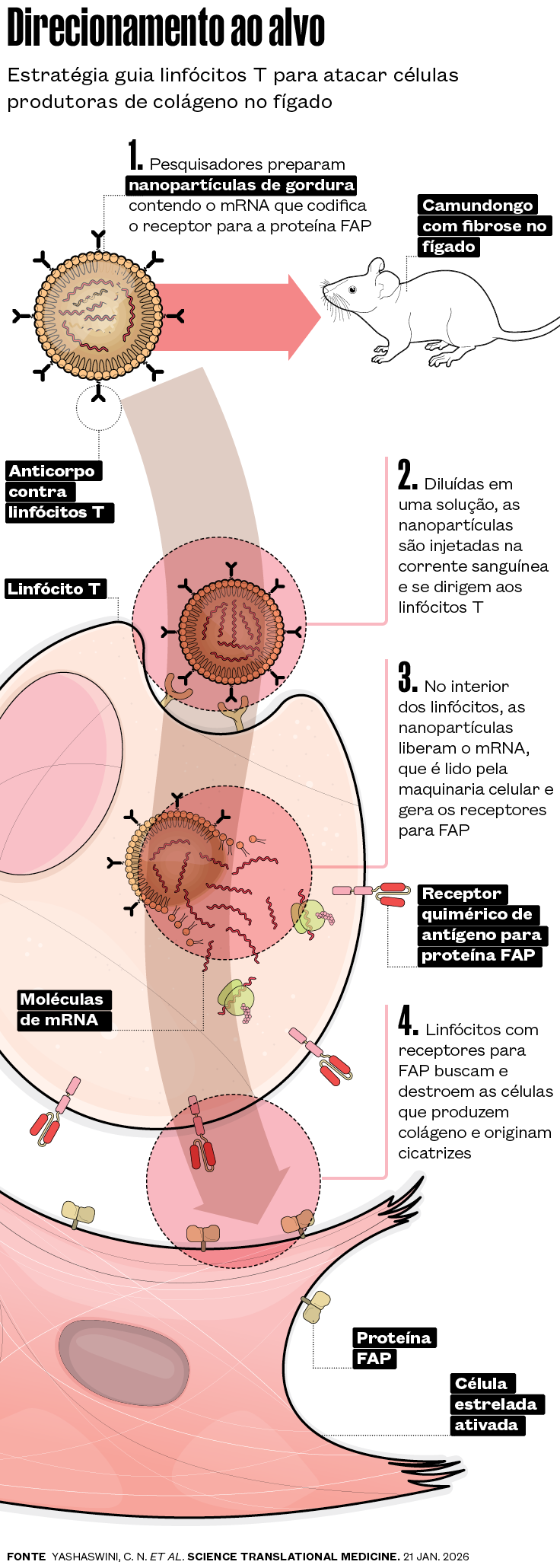
No trabalho publicado em janeiro na Science Translational Medicine, Cogliati e colaboradores testaram outra saída. Em vez de extrair os linfócitos e alterá-los em laboratório, optaram por modificá-los diretamente no organismo dos roedores. Para isso, usaram uma estratégia semelhante à adotada nas vacinas de RNA mensageiro (mRNA) contra a Covid-19. Inseriram cópias de um mRNA que codifica o receptor quimérico da proteína FAP – o ímã – no interior de diminutas gotículas de gordura (nanopartículas lipídicas) recobertas por anticorpos com atração por linfócitos T (ver infográfico abaixo).