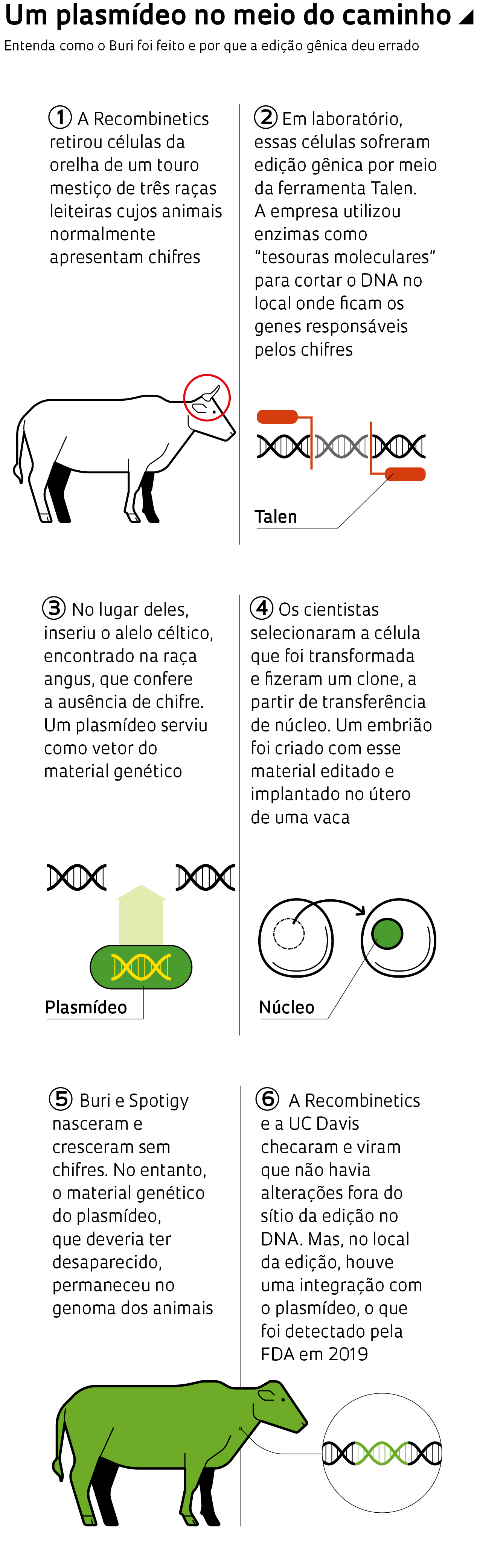
O artigo, assinado pelo pesquisador norte-americano Daniel F. Carlson e colegas, descrevia a bem-sucedida experiência de edição gênica desenvolvida nos animais pela Recombinetics, baseada em Minnesota (EUA). Esse trabalho resultou em dois touros mestiços de raças leiteiras, usualmente com chifres, que atingiram a idade madura sem chifres, ou seja, mochos. As variantes genéticas associadas à ausência de chifres são comuns no gado de corte, mas raros no rebanho de leite. Há um grande apelo comercial para a produção de gado leiteiro mocho, porque os chifres dificultam o manejo dos animais e, muitas vezes, os produtores optam por fazer a descorna, um processo custoso, delicado e doloroso.
GLOSSÁRIO Edição gênica: trata-se de um grupo de tecnologias que dá aos cientistas a capacidade de mudar o DNA de um organismo. Por meio delas, é possível acrescentar, remover ou alterar o material genético em pontos específicos do genoma
Talen: uma das ferramentas de edição gênica, funciona como uma tesoura molecular que corta a fita dupla de DNA em locais específicos
CRISPR-Cas9: ferramenta mais rápida, barata e precisa do que a Talen. Foi adaptada do sistema de defesa que ocorre naturalmente em bactérias para protegê-las de infecção viral
Organismo geneticamente modificado (OGM): é aquele cujo material genético (DNA/RNA) tenha sido modificado por qualquer técnica de engenharia genética
Transgenia: processo no qual se altera o material genético de um organismo com a inclusão de uma ou mais sequências de genes de uma espécie diferente da do organismo modificado
Técnicas Inovadoras de Melhoramento de Precisão (TIMPs): conjunto de metodologias e abordagens que diferem da estratégia de engenharia genética por transgenia por resultar na ausência de DNA ou RNA recombinante no produto final
“Como nosso processo foi desenhado para detectar mudanças no DNA em amostras com edição genômica, queríamos um conjunto de dados para validação que tivesse tanto as amostras editadas quanto as amostras-controle”, contou Lombardi. “O conjunto de dados de autoria de Carlson e equipe foi escolhido para validação porque tinha resultados conhecidos. Era o único conjunto de informações publicamente disponível sobre animais com edição genômica naquela época sobre o qual tínhamos conhecimento. Além disso, os dados eram de boa qualidade e extensos.”
Ocorre que, entre maio de 2015, quando os dois bezerros, chamados Spotigy e Buri, vieram ao mundo, até 2019 muita coisa aconteceu. E a história teve repercussões inclusive no Brasil. Os animais, ambos clones de um mesmo touro da Universidade de Minnesota, cresceram saudáveis, assim como os bezerros usados como controle, que não tiveram o genoma editado. Em novembro de 2015, com cerca de seis meses, foram levados para o campus da Universidade da California (UC), em Davis, para fins de pesquisa. Spotigy foi sacrificado para ter seu organismo estudado, enquanto Buri teve o sêmen congelado e, via inseminação artificial, foi pai de seis bezerros – cinco machos e uma fêmea. A prole nasceu em setembro de 2017 na UC Davis, de seis vacas diferentes da raça hereford, que naturalmente tem chifre. Quatro dos seis bezerros herdaram a sequência com DNA bacteriano no genoma.
Um artigo analisando o genótipo e o fenótipo desses animais, que herdaram a característica mocha de Buri, foi publicado em outubro de 2019 pela revista Nature Biotechnology. O estudo foi coordenado pela pesquisadora australiana radicada nos EUA Alison L. Van Eenennaam, da UC Davis, e teve apoio do Departamento de Agricultura dos Estados Unidos e da Recombinetics.
No primeiro semestre de 2018, antes da divulgação da descoberta da FDA, a empresa paulista AgroPartners Consulting, de Araçatuba, que presta consultoria na área de genômica em plantas e animais, propôs à Recombinetics trazer o sêmen do touro Buri ao Brasil. “A ideia era inseminar algumas vacas, criar um case e fazer uma demonstração dessa tecnologia no país”, contou o veterinário José Fernando Garcia, sócio da AgroPartners e professor da Faculdade de Medicina Veterinária da Universidade Estadual Paulista (Unesp), campus Araçatuba.
Em 2018, a AgroPartners submeteu uma carta-consulta à Comissão Técnica Nacional de Biossegurança (CTNBio) com o objetivo de importar o sêmen de Buri para fazer pesquisas e abrir a possibilidade para futura comercialização desse tipo de tecnologia a outras empresas. Em janeiro daquele ano, a CTNBio havia aprovado a resolução normativa número 16, estabelecendo requisitos para as Técnicas Inovadoras de Melhoramento de Precisão (TIMPs) – nas quais a edição gênica de Buri se enquadraria – e diferenciando estas da engenharia genética por transgenia.
A CTNBio concluiu que o sêmen de Buri não era um organismo geneticamente modificado (OGM), de acordo com o que é descrito no artigo 3º da Lei nº 11.105 de março de 2005, a Lei de Biossegurança. A comissão levou em consideração os dados disponíveis até aquele momento, ressaltando que a mudança inserida – o silenciamento do gene responsável pela ocorrência de chifres – acontece naturalmente em outras raças bovinas.
Projeto abortado
A AgroPartners preparava-se para importar o sêmen quando foi anunciada a descoberta da agência regulatória norte-americana. “A empresa paulista ficou sabendo do achado da FDA e informou à CTNBio, solicitando o cancelamento do processo e informando que não importaria o sêmen do touro”, disse a veterinária Maria Lúcia Zaidan Dagli, professora da Faculdade de Medicina Veterinária e Zootecnia da Universidade de São Paulo (USP) e relatora do processo na CTNBio, da qual é vice-presidente.
De acordo com Garcia, o sêmen do Buri não chegou a ser enviado ao Brasil. Nos Estados Unidos, cinco dos seis descendentes do touro geneticamente modificados foram sacrificados. Apenas a fêmea, Princess, que herdou a sequência com DNA bacteriano no genoma, ainda vive, para continuar como objeto de pesquisa. “Ela está com um touro da raça hereford e esperamos que esteja prenhe”, contou Van Eenennaam, da UC Davis. “Testaremos o leite para análise de composição, como sugerido pela FDA. Tanto a Princess quanto o bezerro dela serão tratados como novas drogas animais [new animal drugs], de acordo com as regras da agência e não poderão entrar na cadeia alimentar. Eles serão sacrificados e incinerados.”
A pesquisa e a comercialização de organismos transgênicos seguem em geral normas regulatórias restritas, que diferem de país a país. Segundo a Organização Mundial da Saúde (OMS), embora as discussões abranjam vários aspectos da transgenia, três pontos são motivos de debate: os possíveis efeitos alergênicos desses organismos; a possibilidade de transferência de material genético, em especial de genes de resistência a antibióticos; e os riscos de cruzamento sem controle desses organismos com outros não transgênicos.
Edição com talen
A Recombinetics usou na edição gênica das linhagens celulares dos touros uma técnica conhecida como Talen, sigla que significa nuclease efetora semelhante a ativadores de transcrição. Outra técnica de edição bastante adotada atualmente, mais simples, rápida e barata, é a CRISPR-Cas9. As duas permitem fazer uma alteração direcionada em um gene ou em uma região específica do genoma, inativando características ou inserindo modificações.
“Ambas funcionam como uma tesoura molecular. Elas cortam o DNA”, explica a bióloga Ângela Saito, pesquisadora do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM). “Mas a Talen usa proteínas modificadas para reconhecer uma sequência específica no DNA de interesse; no caso da CRISPR, o que reconhece a região de interesse é uma molécula de RNA [ácido ribonucleico], cuja construção é mais rápida e simples do que ‘engenheirar’ uma proteína.”
Tanto a Talen quanto a CRISPR-Cas9 podem usar ou não plasmídeos como modelos, que transportam as instruções genéticas. Apesar de o plasmídeo ser uma ferramenta comum nos laboratórios de biotecnologia, muitos pesquisadores preferem sintetizar o modelo de forma que ele seja degradado e, assim, não sobre resquício dele nem se corra o risco de ser incorporado ao DNA.
“Em 2013, tivemos de usar um vetor com plasmídeo porque não havia ainda opções para fazer cópias exatas do alelo céltico [uma inserção de 212 pares de base e uma deleção de 10 pares de base]”, disse à Pesquisa FAPESP Daniel Carlson, diretor científico da Recombinetics, referindo-se à mudança no genoma bovino que garantiu a ausência de chifres nos touros. “Em 2014, quando fizemos o screening [rastreamento] das células editadas, o laboratório não procurou diretamente pelo plasmídeo. A integração de um modelo com plasmídeo era então considerada – e ainda é – um evento raro, conforme a literatura científica.”
Tanto a Recombinetics como a UC Davis não chegaram a buscar especificamente pela integração do plasmídeo antes da descoberta da agência FDA. No caso do Buri, a alteração inesperada do genoma do touro ocorreu em um dos alelos do gene responsável pela presença ou ausência de chifres. No outro alelo, a alteração se deu da maneira como os cientistas previam e queriam. Cada gene que determina um fenótipo (uma característica) possui dois alelos, que podem ser idênticos (homozigotos) ou não (heterozigotos). Se não forem idênticos, o alelo dominante vai determinar a característica apresentada.
Com o alelo céltico dominante, Buri e seu irmão não apresentaram chifres. Mesmo a prole de Buri, fruto de um cruzamento com vacas da raça hereford, em geral com a presença de chifres, nasceu mocha. No entanto, o outro alelo do mesmo gene responsável pela presença ou ausência de chifres sofreu a alteração inesperada contendo, em sua sequência, o DNA bacteriano integrado.
Em geral, os plasmídeos usados como vetores nos laboratórios de biologia molecular têm genes que conferem resistência a antibióticos. E esse foi o caso do material genético integrado ao touro Buri, que incluiu os genes de resistência a antibióticos. Especialistas da Recombinetics, UC Davis, CTNBio e AgroPartners não veem problema nisso. “Os fragmentos do plasmídeo possuem genes bacterianos que não funcionam no organismo de um mamífero. Os genes só funcionam na bactéria, porque ela reconhece aquele gene como seu e faz a resistência a antibiótico”, afirma Garcia, da AgroPartners. “No bovino, o gene está lá como fragmento inerte. O código é diferente, não tem a maquinaria de região promotora necessária para a expressão do gene.”
O veterinário Marcelo Demarchi Goissis, pesquisador da Faculdade de Medicina Veterinária e Zootecnia da USP, concorda com Garcia, mas ressalva: “Em teoria, esse gene está ali quieto, mas trata-se de biologia; e a gente sabe que a biologia tem um quê de imprevisto”, diz. “A princípio não teria problema, mas o ideal seria não ter havido a integração do DNA do plasmídeo ao genoma bovino, porque é difícil prever o que aconteceria com uma população de animais.”
Reportagem sobre o assunto da revista norte-americana MIT Technology Review, do Massachusetts Institute of Technology (MIT), diz que não está claro se a presença do DNA bacteriano significa necessariamente um risco maior. Embora seja improvável que o plasmídeo afete o próprio bovino ou a pessoa que coma a sua carne, a preocupação é de que o gene para resistência a antibiótico seja passado para um dos bilhões de bactérias presentes no corpo do touro ou da vaca. A presença desse gene em uma vaca criaria oportunidades imprevisíveis para a sua disseminação, contou à revista o microbiologista John Heritage, da Universidade de Leeds, no Reino Unido.
De acordo com a Recombinetics, nunca foi intenção da empresa obter a aprovação desse animal pela FDA para a venda nos Estados Unidos ou em outro país. “A base genética do Buri não tem valor comercial, portanto buscar aprovação regulatória não fazia nenhum sentido comercial”, conta Carlson. Para Van Eenennaam, da UC Davis, Buri foi um protótipo para testar se a edição poderia resultar numa característica dominante de ausência de chifres no touro. O próximo passo lógico seria introduzir essa edição em um touro de elite de uma raça com chifre usando métodos que não envolvam DNA com um doador plasmídeo.
Na visão de José Fernando Garcia, o caso foi um “engasgo científico”. “Na nossa opinião, não há grandes problemas. Já há outros animais cujo genoma foi editado, tanto nos Estados Unidos quanto no Brasil, vindo por aí, prestes a nascer. Esses animais e seus dossiês serão submetidos à CTNBio, de forma natural, transparente, como foi feito até agora.”
Artigos científicos
CARLSON, D. F. et al. Production of hornless dairy cattle from genome-edited cell linhas. Nature Biotechnology. n. 5, p. 479-81. 2016.
YOUNG, A. E. et al. Genomic and phenotypic analyses of six offspring of a genome-edited hornless bull. Nature Biotecnolgy. Out. 2019.
NORRIS, A. L. et al. Template plasmid integration in germline genome-edited cattle. bioRxiv. On-line. 28 jul. 2019.
Republicar