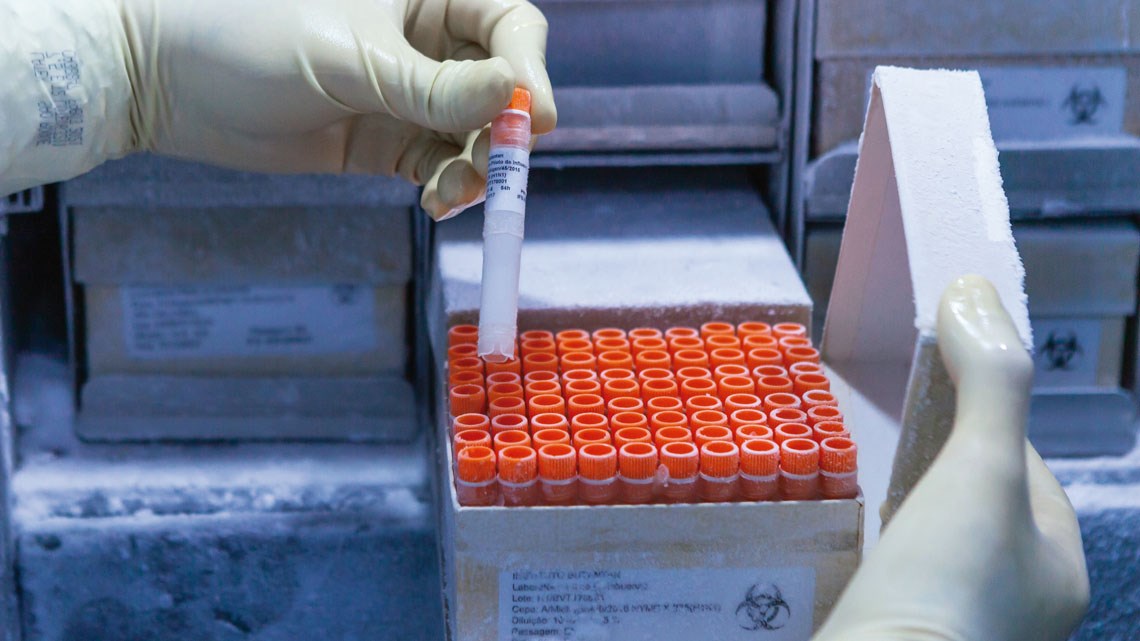
Em 3 de outubro, a Agência Nacional de Vigilância Sanitária (Anvisa), órgão responsável pelo controle de alimentos e medicamentos no país, autorizou o início dos testes em seres humanos da primeira formulação candidata a vacina contra a Covid-19 desenvolvida integralmente no Brasil. É o composto conhecido pela sigla SpiN-Tec-MCTI-UFMG. Criado por pesquisadores do Centro de Tecnologia de Vacinas (CTVacinas) da Universidade Federal de Minas Gerais (UFMG), o candidato a imunizante deve começar a ser administrado em voluntários ainda este ano. O teste será realizado em Belo Horizonte, em duas etapas, envolvendo um total de 432 participantes.
Na primeira delas, a fase 1 do ensaio clínico, 72 voluntários adultos já imunizados contra o novo coronavírus serão separados em três grupos para receber a formulação da UFMG como dose de reforço. Nesse estágio, será feita a aplicação de uma dose baixa, intermediária ou alta. A meta é verificar se o uso do composto é seguro e definir qual concentração desperta a maior resposta imunológica. Se tudo sair como o esperado, em uma etapa seguinte, a fase 2, prevista para começar em fevereiro do próximo ano, outras 180 pessoas, também já vacinadas contra o Sars-CoV-2, receberão uma dose da SpiN-Tec. Seus níveis de anticorpos e a resposta de suas células de defesa (linfócitos T) serão confrontados com os de um número igual de participantes tratados com uma aplicação de reforço de uma vacina já em uso no Brasil. Nesse estágio, o objetivo será investigar se o composto da UFMG não induz resposta imune inferior à do imunizante amplamente adotado e, assim, abrir caminho para a última etapa de avaliação em seres humanos, a fase 3.
“O Brasil nunca fez uma vacina para uso humano a partir do zero”, conta o imunologista Ricardo Gazzinelli, coordenador do CTVacinas e líder da equipe que desenvolveu a SpiN-Tec. “Temos grande expectativa de que dê certo, mas, ainda que essa formulação não se torne um produto comercial imediatamente, aprendemos a desenvolver imunizantes seguindo as exigências de segurança e qualidade das agências reguladoras. Isso deve nos habilitar para criar vacinas contra outras doenças”, completa.
Com a SpiN-Tec, agora são três as candidatas a vacina em teste clínico no Brasil que contaram com algum nível de colaboração nacional em seu desenvolvimento. As outras duas são a RNA-MCTI-Cimatec-HDT e a ButanVac. A primeira foi elaborada pela empresa norte-americana HDT Biotech Corporation, de Seattle, com a participação de pesquisadores do centro de ensino, pesquisa e desenvolvimento tecnológico Senai-Cimatec, na Bahia. Já a segunda utiliza uma plataforma concebida por equipes da rede de hospitais Monte Sinai, em Nova York, e é desenvolvida por um consórcio internacional integrado pelo Instituto Butantan. Ambas já concluíram os ensaios clínicos de fase 1 e submeteram os resultados à Anvisa, que, em 7 de outubro, aprovou o avanço da formulação da Cimatec-HDT para a etapa seguinte. O Butantan aguarda a análise, prevista para ocorrer ainda em outubro, das últimas informações solicitadas pela agência para liberar o início da fase 2 com a ButanVac.
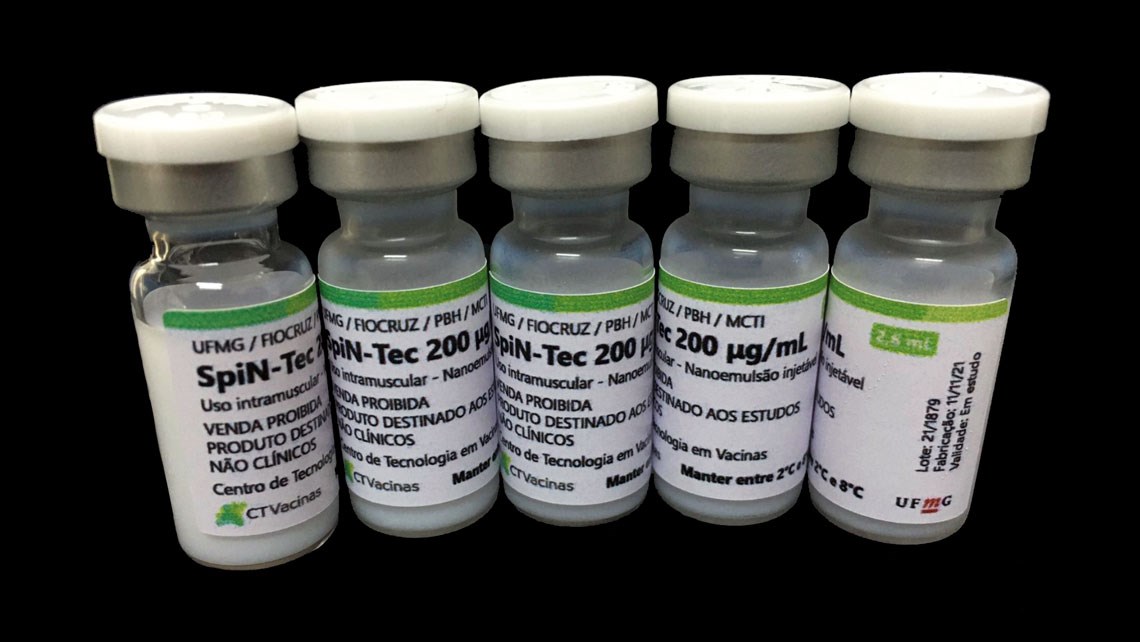
CTVacina / UFMGLote da SpiN-Tec, desenvolvida na UFMG, destinado a ensaio clínicoCTVacina / UFMG
A tentativa de obter uma vacina criada total ou parcialmente no Brasil é parte de um esforço nacional para dominar todas as etapas da extensa e complexa cadeia de fabricação de produtos imunobiológicos. No país, vários grupos de pesquisa realizam os estágios iniciais da produção de um imunizante, da formulação do princípio ativo à realização dos experimentos com animais. Isso, no entanto, não é suficiente para chegar a um produto que possa ser aplicado no braço das pessoas. Faltam elos nessa cadeia. Um deles é a ausência de centros com a capacidade de ampliar a escala de produção dos compostos seguindo as boas práticas de fabricação para iniciar os testes clínicos. “Não temos no Brasil a expertise da parte de desenvolvimento industrial”, afirma o imunologista Jorge Kalil, do Instituto do Coração (InCor) do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (USP), coordenador do desenvolvimento de uma formulação de uso nasal contra a Covid-19 que já concluiu os testes em animais.
Desde o início de 2020, o novo coronavírus já infectou 620 milhões de pessoas no mundo e matou 6,5 milhões, segundo números da Organização Mundial da Saúde (OMS). Os especialistas apostam que o vírus veio para ficar e, após a fase inicial, na qual pegou a população desprotegida, deve passar a se comportar agora como o vírus da gripe, causando surtos nos meses frios. Esse padrão deve exigir o uso de doses de reforço dos imunizantes, que ainda precisam ser mais eficazes e geradores de proteção mais duradoura.
Risco de dependência
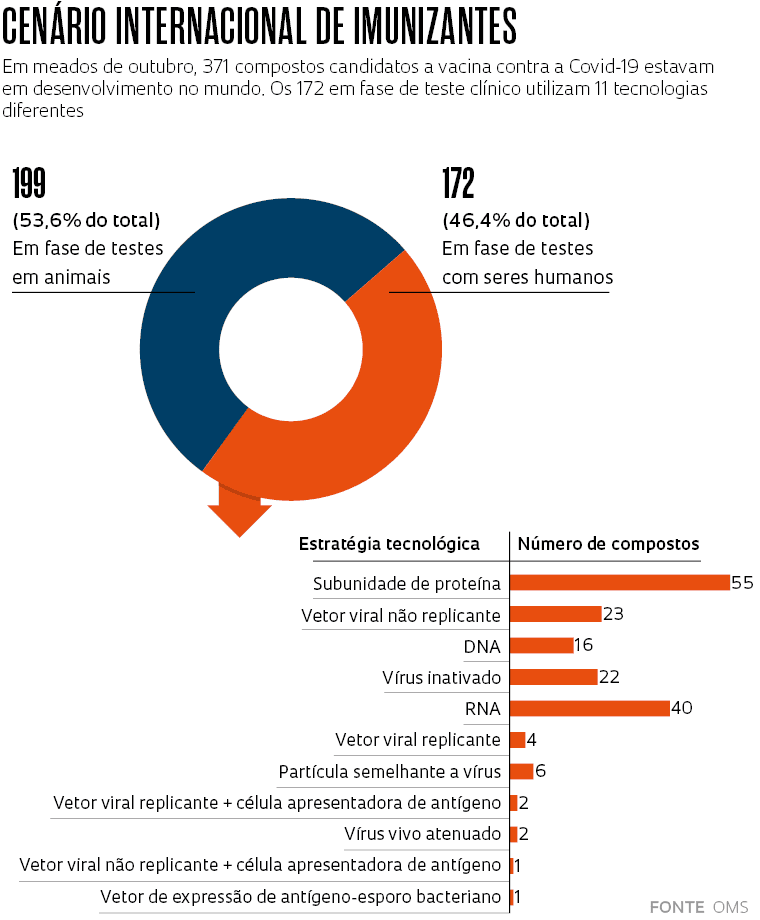
Por essa razão, apesar de haver quase 50 vacinas já aprovadas para uso humano no mundo, a OMS registrava em outubro outros 371 compostos candidatos a imunizantes contra o Sars-CoV-2 em desenvolvimento (ver gráfico). Com a pandemia, dizem especialistas da área, houve uma revolução nas tecnologias de produção de vacinas e o país que não as dominar pode se tornar dependente de importações.
Os três compostos com alguma participação nacional que alcançaram a etapa de experimentação em seres humanos utilizam tecnologias distintas para ativar o sistema de defesa.
Desenvolvida com apoio do MCTI, da FAPESP e da Fundação de Amparo à Pesquisa de Minas Gerais (Fapemig), a SpiN-Tec não estimula apenas a produção de anticorpos contra a proteína da espícula, ou spike (S), do Sars-CoV-2, como faz a maioria das vacinas disponíveis no mercado. Além dessa proteína, que fica na superfície do vírus exposta ao ataque de anticorpos e sofre alterações com frequência, a equipe de Minas acrescentou a proteína N, do nucleocapsídeo, o envoltório que protege o material genético viral e quase não muda de uma cepa para outra. Sintetizada por bactérias, a proteína híbrida – SpiN – é depois purificada e misturada a uma emulsão de compostos oleosos que favorecem a ativação de células de defesa e amplificam a resposta imunológica.
Nos testes de eficácia em modelos animais, feitos na USP de Ribeirão Preto em colaboração com a equipe do imunologista João Santana da Silva e a do virologista Luiz Tadeu Figueiredo, a vacina foi administrada em duas espécies de roedores (camundongo e hamster). Em todos os animais, o imunizante baseado na proteína SpiN ativou uma resposta imunológica potente. Segundo resultados publicados em agosto na revista Nature Communications, a SpiN-Tec estimulou tanto a ativação de linfócitos T, células que combatem diretamente o vírus e as células infectadas, quanto a dos linfócitos B, produtores de anticorpos. Aplicada em duas doses, a SpiN-Tec evitou o adoecimento em um tipo de roedor que serve de modelo para doença leve e em outro que simula a grave, quer contra o Sars-CoV-2 original, quer contra as variantes delta e ômicron.
“A vacina baseada na proteína SpiN não induz, por si só, a produção de anticorpos neutralizantes”, explica Gazzinelli, que também é pesquisador da Fundação Oswaldo Cruz (Fiocruz) em Minas Gerais e professor visitante na USP em Ribeirão Preto, por onde recebeu auxílio da FAPESP. “Mas, usada como dose de reforço, ela estimula a capacidade de produzir anticorpos gerada por vacinação anterior, bem como a imunidade celular, conferindo dupla proteção.”
Em fase mais avançada de testes em voluntários, o composto da dupla Cimatec-HDT funciona com base em uma tecnologia de RNA diferente da empregada nas vacinas da Pfizer-BioNTech e da Moderna. Em vez de usar a molécula de RNA mensageiro para levar às células a receita da proteína S, a formulação do Cimatec-HDT emprega moléculas de RNA contendo um trecho especial – o RNA replicante. Esse RNA híbrido se multiplica no interior das células várias vezes antes de iniciar a produção da proteína da espícula. Realizado em Seattle, o desenvolvimento do RNA replicante e das nanopartículas de lipídios que o envolvem contou com a participação do infectologista Roberto Badaró e da bioquímica Bruna Machado, do Senai-Cimatec. “Desde antes da pandemia, eles já colaboravam com a HDT no desenvolvimento dessa plataforma tendo como alvo doenças como a zika”, conta Valdir Gomes Barbosa, gestor de negócios do centro baiano. “Nos testes pré-clínicos contra o coronavírus, feitos nos Estados Unidos, essa tecnologia gerou uma resposta imune consistente com doses muito baixas”, relata. A tecnologia já foi incorporada pelo Senai-Cimatec, que dominou a produção em escala laboratorial.
Na primeira fase de ensaio clínico, financiada pelo MCTI e realizada no início do ano em Salvador, a formulação foi administrada a 90 voluntários adultos já previamente imunizados contra a Covid-19 com outras vacinas. Eles foram divididos em três grupos: um recebeu duas aplicações de 1 micrograma (µg), outro de 5 µg ou um terceiro de 25 µg. Segundo Barbosa, os resultados, já apresentados à Anvisa, mostraram que o composto é seguro e não causa efeitos adversos graves, o que motivou a liberação para a fase 2. Nessa etapa, planejada para iniciar em meses, metade dos 330 voluntários deverá receber duas doses de 5 µg ou 10 µg, definidas a partir de ensaios clínicos em andamento nos Estados Unidos, na Índia e na Coreia do Sul. A outra metade será tratada com duas doses da vacina da Pfizer-BioNTech.

Nalini Vasconcelos / Senai-CimatecPesquisador realiza inspeção visual de frasco da formulação Cimatec-HDTNalini Vasconcelos / Senai-Cimatec
A ButanVac, por sua vez, usa o vírus da doença aviária de Newcastle, praticamente inofensivo para os seres humanos, para introduzir no organismo uma versão mais estável da proteína S (ver Pesquisa FAPESP nºs 302 e 303). Ela foi concebida na Escola de Medicina Icahn, da rede Monte Sinai de hospitais de Nova York, para gerar um produto barato e que pudesse ser sintetizado em fábricas de vacina da gripe. Autorizados pela Anvisa em julho de 2021, os testes de fase 1 avaliaram o desempenho do composto em 318 participantes em Ribeirão Preto, interior de São Paulo. Eles foram separados em grupos menores, que receberam duas doses de 1 µg, 3 µg ou 10 µg. “Observamos uma resposta humoral [produção de anticorpos] marcante, em especial com a dose mais alta”, conta Érique Miranda, gestor médico de Desenvolvimento Clínico no Setor de Ensaios Clínicos do Instituto Butantan.
Duas semanas após a aplicação da segunda dose, a ButanVac elevou em mais de quatro vezes a produção de anticorpos em 98,7% dos participantes. Não houve efeitos adversos graves. Os problemas mais comuns foram dor no local da aplicação, em 89% dos casos, dor de cabeça (67%), cansaço (65%), dores no corpo (58%) e febre (17%). “Foram resultados muito semelhantes aos verificados no estudo clínico com a mesma formulação feito na Tailândia”, afirma Miranda. Os dados do ensaio feito no país asiático foram publicados na forma de preprint em setembro de 2021 e sugerem que a formulação também desperte a resposta celular. Assim que autorizado, o Butantan deve iniciar os testes com outros 400 voluntários em São Paulo e no Rio de Janeiro.
Os três compostos – SpiNTec, Cimatec-HDT e ButanVac – são sobreviventes da longa corrida de obstáculos que deixa muitos competidores pelo caminho. No Brasil, ainda em 2020, instituições de financiamento à pesquisa federais e estaduais começaram a investir recursos no desenvolvimento de potenciais imunizantes contra a Covid-19. O MCTI financiou o desenvolvimento inicial de 16 compostos, cujo princípio ativo tivesse sido desenvolvido por pesquisadores em institutos brasileiros ou em parceria internacional que resultasse na transferência da tecnologia para o país. “Somos bons em trazer tecnologia externa e produzir no Brasil, mas nunca fizemos uma vacina do começo ao fim. Decidimos estimular o desenvolvimento de competência nacional para a produção de imunizantes”, afirma Marcelo Morales, secretário de Pesquisa e Formação Científica do Ministério da Ciência, Tecnologia e Inovações (MCTI), a seção da pasta que estimulou o desenvolvimento no país de alguns potenciais imunizantes contra a Covid-19.
Dos 16 compostos, cinco concluíram os experimentos com animais e se candidataram a compartilhar os R$ 115 milhões destinados aos testes de fase 1 e 2, entre eles a formulação da HDT-Cimatec e a da UFMG. Duas outras estão aptas a receber o financiamento para os ensaios clínicos, assim que receberem a aprovação da Anvisa para começar os testes em humanos: a MultiCovax, criada pela equipe de Kalil, no InCor; e a Versamune-CoV-2F, formulada pelo imunologista Célio Lopes Silva, da USP em Ribeirão Preto, em parceria com a empresa paulista Farmacore e o laboratório norte-americano PDS Biotechnology. “Mostramos que nosso composto gera altos níveis de anticorpos e resposta celular na mucosa nasal nos testes com animais”, relata Kalil. Seu grupo agora enfrenta o desafio de obter o primeiro lote-piloto para aplicação em voluntários, que terá de ser feito no exterior, a um custo de US$ 4 milhões, por causa da ausência de empresas aptas no país. Na Universidade Federal do Rio de Janeiro (UFRJ), o grupo da engenheira bioquímica Leda Castilho corre para concluir a fase de testes em animais da formulação UFRJVac ainda este ano.
Projeto
Vacina intranasal bivalente utilizando vírus influenza expressando a proteína S (spike) do SARS-CoV-2: mecanismos de proteção e lesão pulmonar (nº 20/05527-0); Modalidade Auxílio à Pesquisa – Regular; Pesquisador responsável Ricardo Tostes Gazzinelli (USP); Investimento R$ 283.052,33.
Artigos científicos
CASTRO, J. T. et al. Promotion of neutralizing antibody-independent immunity to wild-type and SARS-CoV-2 variants of concern using an RBD-nucleocapsid fusion protein. Nature Communications. 17 ago. 2022.
PITISUTTITHUM, P. et al. Safety and immunogenicity of an inactivated recombinant Newcastle disease virus vaccine expressing Sars-CoV-2 spike: Interim results of a randomised, placebo-controlled, phase 1/2 trial. MedRxiv. 20 set. 2021.
Republicar