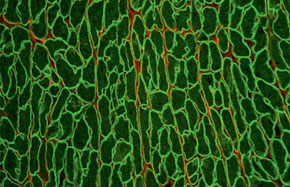
Marcos Rossi y Érica Carolina Campos / USP-RPCorazón seccionado: la estructura formada por la proteína distrofina (en verde)…Marcos Rossi y Érica Carolina Campos / USP-RP
Investigadores de la Facultad de Medicina de Ribeirão Preto en la Universidad de São Paulo (FMRP-USP) concretaron dos importantes hallazgos en un mismo estudio. En primer lugar, identificaron la probable causa de los problemas cardíacos que afectan a los individuos tratados con doxorrubicina, un antibiótico naturalmente producido por bacterias y ampliamente utilizado para combatir algunos de los tipos más comunes de cáncer. En experimentos con ratas, verificaron que ese compuesto destruye la distrofina, una proteína que mantiene la elasticidad y permite la contracción de las células cardíacas. En el mismo trabajo, la investigadora Érica Carolina Campos, del equipo del patólogo Marcos Rossi, encontró una forma prometedora para mitigar los daños provocados por la doxorrubicina en el corazón.
La doxorrubicina es un compuesto derivado de las antraciclinas, aisladas en la década de 1960 a partir de la bacteria Streptomyces peucetius. Desde entonces ha sido utilizada como quimioterapéutico en función de su amplio espectro de actuación. “Las antraciclinas ocasionan daños irreversibles en las células tumorales ya que interfieren en el ADN, inhiben la síntesis de proteínas y producen especies reactivas de oxígeno, provocando la muerte celular”, explica Rossi. “Por eso, siempre se las consideró uno de los medicamentos más eficaces para el tratamiento de tumores en humanos”.
No obstante, con el tiempo se verificó que la doxorrubicina produce efectos colaterales que resultan cada vez más intensos. El principal es la dilatación del corazón, lo cual causa insuficiencia cardíaca y puede conducir a la muerte. La insuficiencia puede ser aguda, observada luego de suministrar la primera dosis al paciente y tratable fácilmente, o crónica, que se manifiesta durante el transcurso de meses de tratamiento. La estrategia actual para intentar reducir los daños cardíacos consiste en limitar la dosis de la medicación a valores entre 500 y 550 miligramos por metro cuadrado (mg/m2) de superficie corporal. Un individuo con una estatura de 1,80 m y 80 kilogramos de peso cuenta con unos 2 m2 de superficie corporal y puede recibir una dosis acumulativa máxima entre 1.000 y 1.100 mg. De todos modos, no se logra evitar completamente sus efectos tóxicos. “Se estima que entre un 5% y un 35% de los pacientes que reciben dosis superiores a 400 mg/m2 de antraciclinas presentan un descenso en los índices de la función cardíaca o incluso insuficiencia cardíaca”, dice Rossi.

Marcos Rossi y Érica Carolina Campos / USP-RP…dañada por la doxorrubicina en la imagen arribaMarcos Rossi y Érica Carolina Campos / USP-RP
Algunas hipótesis procuraban explicar el origen de los daños que la doxorrubicina provoca en las células del corazón (cardiomiocitos). El más estudiado de ellos es el estrés oxidativo. Según los defensores de esa idea, las antraciclinas generan radicales libres, moléculas altamente reactivas que causarían lesiones en la membrana y en otros componentes de las células. “Pero este mecanismo ha sido cada vez más cuestionado”, comenta Rossi. “Por ello ha aumentado nuestro interés por estudiar la causa de la lesión cardíaca, lo que nos permite plantear que ésta es consecuencia de daños en las proteínas estructurales de los cardiomiocitos, principalmente la distrofina”.
Para probar esa hipótesis, Campos trató durante dos semanas a tres grupos de ratas con diferentes dosis de doxorrubicina y analizó lo que ocurría con el corazón de los roedores. “Evaluamos la expresión de las proteínas en las células del corazón y también la función cardíaca 7 días y 14 días después de la última dosis suministrada”, relata Campos.
Ella verificó una significativa pérdida de distrofina en las células cardíacas. Cuanto mayor era la dosis del medicamento, menos distrofina había en el corazón y la tasa de mortalidad entre los animales era mayor, según refirieron los investigadores en un artículo en el European Journal of Pharmacology. Exámenes por imágenes, tales como la ecocardiografía, también revelaron que la pérdida de distrofina dañó la capacidad de bombeo de la sangre. “Fue considerada la causa estructural responsable de la pérdida de la función cardíaca”, sostiene Campos.
Pero no bastaba con confirmar su efecto nocivo. Los investigadores también querían saber cómo se destruía la distrofina a causa de la medicación. “Descubrimos que los daños en la membrana de los cardiomiocitos permiten el ingreso de mayor cantidad de iones de calcio”, explica Rossi. “Eso, simultáneamente, activa a las proteasas (peptidasas, enzimas) que lesionan a las células”.
Al acceder a ese conocimiento, los investigadores comenzaron a buscar formas de reducir los daños cardíacos causados por las antraciclinas. Uno de los compuestos que probaron fue el miorrelajante dantrolene, que reduce la contracción de las células al bloquear la entrada de calcio. Administrado en junto a la doxorrubicina, ese miorrelajante redujo la pérdida de distrofina y los focos de lesión. “Las ratas tratadas con dantrolene y doxorrubicina mantuvieron la función cardíaca en niveles similares a los de los animales del grupo control [a los que se les había suministrado placebo en lugar del quimioterapéutico]”, relata Rossi. “Nuestros hallazgos entusiasman porque promueven la posibilidad de que, en un futuro, quizá se pueda reorientar la práctica clínica”.
El Proyecto
Distrofina y sus proteínas asociadas en la patogénesis de la cardiomiopatía inducida por doxorrubicina (nº 2010/13199-1); Modalidad Apoyo Regular al Proyeto de Investigación; Coordinador Marcos Antonio Rossi – FMRP/USP; Inversión R$ 263.235,82 (FAPESP)
Artículo científico
CAMPOS, E. C. et al. Calpain-mediated dystrophin disruption may be a potential structural culprit behind chronic doxorubicin-induced cardiomyopathy. European Journal of Pharmacology. v. 670(2-3), p. 541-53.30 nov. 2011.