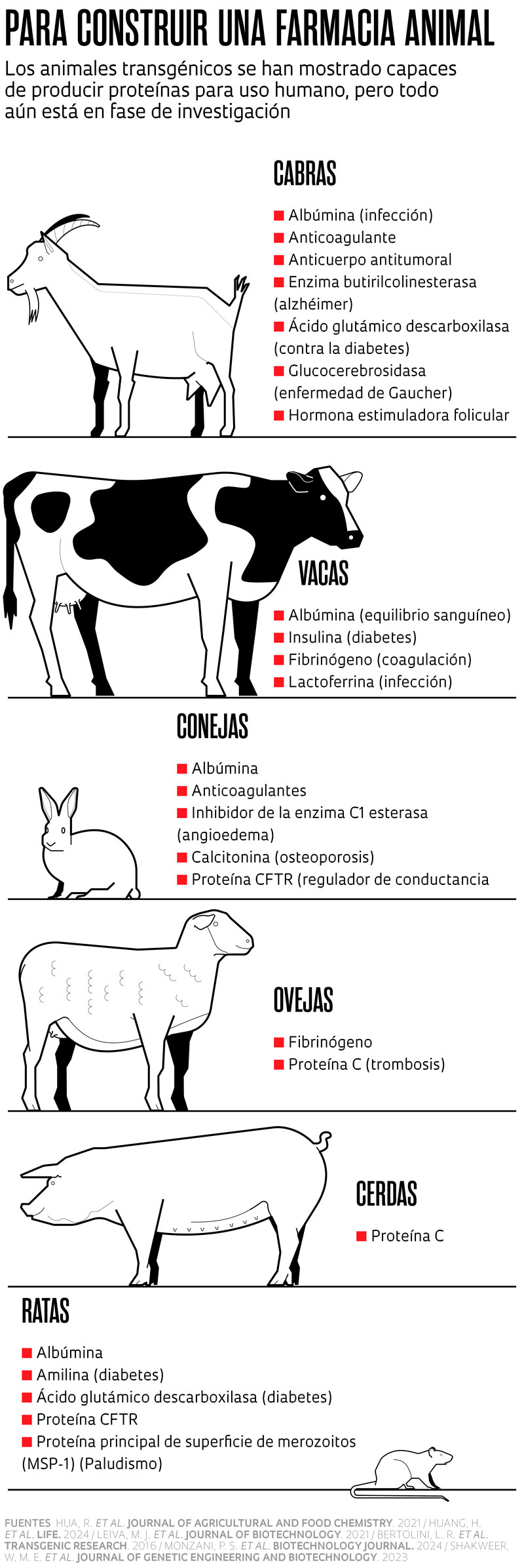
En un artículo científico publicado en marzo de este año en la revista Biotechnology Journal, investigadores de las universidades de São Paulo (USP), do Norte do Paraná (Unopar) y de Illinois, en Estados Unidos, demostraron que una vaca transgénica que desarrollaron produjo leche con insulina humana. La hormona controla los niveles de glucosa en la sangre, esencial para los diabéticos. Esta prueba de concepto no prosperó, pero dejó planteada la posibilidad, ya apuntada por otros grupos de investigación, de producir medicamentos para uso humano en las glándulas mamarias de vacas, cabras y conejas modificadas genéticamente (véase la infografía abajo).
Todavía no se producen medicamentos de este tipo en Brasil. En el exterior, la Agencia Europea de Medicamentos (EMA) y la Food and Drug Administration (FDA), el organismo que regula los alimentos y los medicamentos en Estados Unidos, aprobaron en 2006 y 2009, respectivamente el primer medicamento de este tipo, una antitrombina humana recombinante. Producida con leche de cabras transgénicas por la farmacéutica estadounidense LFB Biotechnology, está recomendada para personas con deficiencia hereditaria de la proteína antitrombina. Esta molécula inhibe la coagulación sanguínea y reduce el riesgo de obstrucción de los vasos sanguíneos y de infarto.
Otra proteína humana recombinante, extraída de la leche de conejas transgénicas, fue aprobada para su venta en Europa en 2012 y en Estados Unidos en 2014. Producido por la empresa holandesa Pharming Group y por la estadounidense Salix Pharmaceutics, el medicamento está recomendado para la forma hereditaria de angioedema, una enfermedad rara causada por una deficiencia en la producción de una proteína sanguínea llamada inhibidor de la enzima C1 esterasa.
Más recientemente, en 2020, la FDA aprobó una proteína, también de LFB, que ayuda a la coagulación de la sangre. Se produce en las glándulas mamarias de conejas transgénicas. Aparte de estos tres medicamentos ya disponibles en el mercado, otras proteínas para uso humano se produjeron experimentalmente en animales, incluso en Brasil.
La historia de la leche transgénica brasileña con insulina humana comenzó en 2008, en la Facultad de Zootecnia e Ingeniería de Alimentos (FZEA) de la USP, en su campus de la localidad de Pirassununga. Allí, el veterinario Flávio Meirelles y el biólogo Paulo Monzani comenzaron a preparar un tipo de cromosoma artificial (plásmido) utilizando el gen que inicialmente podría activar la producción del factor IX de coagulación humano. El plásmido fue implantado en un virus, que se incorporó al ADN de un fibroblasto, un tipo de célula que acepta materiales extraños con relativa facilidad. El fibroblasto genéticamente modificado se fusionó con una célula reproductora femenina, llamada ovocito, sin núcleo, y el embrión que comenzó a formarse se transfirió luego al útero de una vaca. En 1996, un proceso similar había generado la oveja Dolly, el primer animal clonado a partir de una célula adulta de otra oveja.
En 2010 nacieron dos terneras modificadas genéticamente para el factor IX de coagulación humano, pero murieron poco después. Luego, Meirelles y Monzani comenzaron a trabajar con el grupo del veterinario Otávio Mitio Ohashi, de la Unopar, para producir vacas transgénicas capaces de formular fármacos como la insulina humana. En la Unopar, Monzani construyó otros plásmidos, incluidos los de insulina, incorporados por fibroblastos de una vaca de la raza jersey.
“Varias transferencias de embriones no funcionaron”, relata Meirelles. “La clonación tiene baja eficiencia”. Después de varios intentos, en 2014 nació una vaca con el gen de la proinsulina humana y creció en una finca del interior de Paraná, del propietario de la Unopar, Marco Laffranchi (1936-2015). Al no quedar preñada, incluso después de probar diferentes técnicas reproductivas, el animal fue sometido a una inducción hormonal de lactancia y produjo leche con insulina humana. Sin embargo, un imprevisto interrumpió la investigación: “La vaca murió mientras estaba pastando, posiblemente picada por una serpiente, en 2022”, se lamenta Monzani.
Sin financiación, la investigación se detuvo, pero Meirelles sigue convencido de que las glándulas mamarias de vacas, cabras y otros animales de granja pueden constituir un ambiente excelente – o biorreactor, en un lenguaje más formal – para la producción de medicamentos de uso humano: “La proporción de proteínas transgénicas en la leche es del orden de gramos por litro, un rendimiento mucho mayor que el de las técnicas convencionales”.
Las investigaciones que se interrumpen son algo común en este campo. En 2007, un grupo de la empresa argentina Biosidus anunció el nacimiento de cuatro vacas jerseys capaces de producir leche conteniendo insulina humana (lea en Pesquisa FAPESP, edición nº 147). En su momento, se dijo que 25 vacas serían suficientes para abastecer toda la demanda argentina de insulina, con un precio al menos 30 % menor que la producida mediante otras técnicas. Después de 17 años, no hubo más noticias sobre este programa empresarial. Pesquisa FAPESP intentó contactar a los responsables de la empresa, que no se manifestaron.
Lo que se sabe proviene de un informe sobre biotecnología agrícola en Argentina publicado en diciembre de 2022 por el Departamento de Agricultura de Estados Unidos. “Aunque existen regulaciones para la aprobación de animales genéticamente modificados, en la Argentina no existe producción comercial, ni con fines agrícolas, ni para investigación biomédica, producción farmacéutica o producción de órganos para trasplantes”, informa el documento. Asimismo, según el mismo, el interés de los productores por los animales transgénicos ha disminuido en los últimos años, ya que la legislación europea prohíbe la importación de animales o productos transgénicos.
Experimentalmente, la leche de vacas transgénicas también se ha utilizado para producir la hormona del crecimiento humano, albúmina, anticuerpos monoclonales contra el cáncer y proteínas que facilitan la coagulación sanguínea. En general, informes como los del grupo de la USP no hacen referencia al resultado obtenido, pero en 2014 investigadores de la Universidad de Vermont, en Estados Unidos, utilizando ratas transgénicas, obtuvieron 8,1 gramos por litro (g/L) de insulina humana.
Desde el decenio de 1980, esta hormona, esencial para controlar la diabetes, se produce mediante el cultivo de la bacteria Escherichia coli genéticamente modificada. Una de las pocas empresas en el mundo que dominó la técnica de producción de insulina a partir de E. coli fue Biobrás, creada por investigadores de la Universidad Federal de Minas Gerais (UFMG). En 2001, fue adquirida por la empresa danesa Novo Nordisk y, posteriormente, fue desactivada. Los exdirectores de Biobrás crearon Biomm, que importa insulina (lea en Pesquisa FAPESP, edición nº 302). Actualmente, toda la insulina que se consume en Brasil es importada.

Paulo S. MorzaniLa vaca cuya leche contenía insulina humanaPaulo S. Morzani
Con E. coli, el rendimiento es de 0,009 g por litro de medio de cultivo, según un análisis de las técnicas de producción de insulina con microorganismos publicado en octubre de 2014 en la revista Microbial Cell Factories. Otra comparación, publicada en la revista Transgenic Research, de junio de 2016, señala que la misma cantidad de proteína recombinante obtenida de la leche de animales de granja costaría ocho veces menos que la obtenida mediante el cultivo de células de ovario de hámster china, la fuente de la proteína deseada.
“Aunque obtengan buenos resultados iniciales, muchos proyectos se detienen porque son lentos y costosos”, reconoce la veterinaria Maria Angélica Miglino, de la Universidade de Marília (Unimar), en el interior de São Paulo. Ella no participó en el proyecto de la USP, pero hace aproximadamente un año recibió de Monzani una muestra de células epiteliales de glándula mamaria de vaca. Su objetivo es construir en el laboratorio una glándula mamaria artificial, capaz de producir leche y servir como modelo experimental para estudiar enfermedades animales y humanas. Este trabajo forma parte del doctorado del veterinario mozambiqueño Fernando Chissico en la Unimar, bajo la dirección de Miglino.
“El gran problema de las proteínas recombinantes producidas por las glándulas mamarias de los animales no es la tecnología, sino la regulación”, comenta la bióloga brasileña Luciana Relly, directora científica de C&L Biotech, una consultora estadounidense referente a animales transgénicos. “Un medicamento producido por animales transgénicos también debe cumplir con todas las etapas de las pruebas preclínicas y ensayos clínicos y, además, cumplir con los requisitos de producción, garantizando que los animales y las proteínas recombinantes estén libres de cualquier contaminación”.
De 2006 a 2015, en la Universidade de Fortaleza (Unifor), en Ceará, Relly fue una de las coordinadoras de la investigación que culminó con el nacimiento de una cabra transgénica capaz de producir leche con la enzima glucocerebrosidasa, cuya deficiencia provoca la enfermedad de Gaucher (lea en Pesquisa FAPESP, edición nº 236). A pesar de haber sido ampliamente difundido y celebrado, este trabajo no avanzó. “El gobierno federal prefirió negociar la transferencia de la tecnología de producción de una empresa israelí, pero no se avanzó”, explica. Sin ningún tipo de financiación, el grupo de la Unifor se disolvió.
Relly se trasladó a la Pontificia Universidad Católica de Rio Grande do Sul (PUC-RS) en 2015. Cinco años después se mudó a Estados Unidos. Su trayectoria la llevó a formular esta conclusión: “Las glándulas mamarias constituyen un excelente biorreactor, especialmente para proteínas que no podrían producirse de otra manera, como Atryn [el nombre comercial de la antitrombina recombinante de LFB], que es difícil de producir en las células.”
Con lo aprendido durante esta experiencia, los investigadores que continuaron en la Unifor, exalumnos de posgrado de los coordinadores iniciales, ayudaron a sus colegas de la Universidad de Concepción, en Chile, a obtener, a partir de la leche de cabra, un anticuerpo antitumoral llamado inhibidor del factor de crecimiento endotelial vascular (VEGF). Descrito en 2021 en la revista científica Journal of Biotechnology, el proceso refuerza la posibilidad de implementar otras formas de producir medicamentos para uso humano.
Hilos de seda producidos por cabras
Liviano, flexible y resistente, este material podría utilizarse en la fabricación de uniformes militares y en cuerdas para raquetasLas glándulas mamarias de los animales transgénicos no solamente se han investigado para la producción de fármacos. En 2002, la leche de cabra sirvió como ambiente para la fabricación de hilos de seda, después de que investigadores de la empresa canadiense Nexia Biotechnologies implantaron en el animal genes de araña capaces de producirlos. También llamado bioacero, este material resulta interesante porque es liviano, flexible y más resistente que los hilos de acero, con potenciales aplicaciones en uniformes militares, suturas quirúrgicas o cuerdas de raquetas de tenis.
La empresa quebró en 2009, pero el biólogo molecular Randy Lewis, de la Universidad de Wyoming, en Estados Unidos, continuó el trabajo y obtuvo 30 cabras transgénicas, mantenidas en una granja de la Universidad del Estado de Utah, también en Estados Unidos. Según un comunicado de la Universidad de Wyoming de octubre de 2023, solamente tres de cada siete crías de cabras transgénicas tienen el gen de la proteína. Su experiencia motivó a la artista y empresaria holandesa Jalila Essaïdi a crear, en 2011, una empresa con el objetivo de producir ropa antibalas utilizando hilos procedentes de cabras transgénicas. Todavía no existe ningún producto comercial.
Proyecto
Producción de embriones bovinos transgénicos para la elaboración del factor IX de coagulación (nº 08/00102-0); Modalidad Becas en Brasil – Posdoctorado; Investigador responsable Flávio Vieira Meirelles (USP); Beneficiario Paulo Sérgio Monzani; Inversión R$ 126.819,24.
Artículos científicos
BAESHEN, N. A. et al. Cell factories for insulin production. Microbial Cell Factories. v. 13, n. 141. 2 oct. 2014.
BERTOLINI, L. R. et al. The transgenic animal platform for biopharmaceutical production. Transgenic Research. v. 25, p. 329-43. 28 ene. 2016.
Republicar