Eurico de Arruda Neto es un estudioso de los virus, seres situados en la frontera entre lo vivo y lo no vivo, cuya constitución es tan magra que dependen por completo de otros organismos vivos para reproducirse y evolucionar. “Son parásitos bioquímicos sofisticados”, dice el virólogo, cuyo interés por estos seres microscópicos, constituidos básicamente de material genético recubierto por una capa de proteínas, se había despertado durante sus estudios universitarios de grado, cursados en la Universidad Federal de Ceará (UFC), en Brasil.
En el último año de la carrera de medicina, participó en un proyecto de investigadores estadounidenses que estudiaban las infecciones habituales en una favela de Fortaleza (Ceará) y descubrió la importancia de los virus respiratorios para la salud humana, a los que hasta entonces se les prestaba escasa atención. En su maestría en la Universidad Federal de São Paulo (Unifesp), estudió la prevalencia del VIH entre los indígenas brasileños y, durante su doctorado, que inició en la misma institución y luego lo concluyó en la Universidad de Virginia, en Estados Unidos, reanudó la investigación de los virus respiratorios. Cuando estaba allá, hacia el final de la década de 1980, tuvo el primer contacto con los coronavirus, que en aquella época ya se sabía que infectaban a los seres humanos y causaban problemas respiratorios similares a las gripes o los resfriados.
Desde entonces, estos virus, causantes de alrededor del 10 % de las afecciones respiratorias en adultos y niños, ya no han salido de su radar. La pandemia de covid-19 causada por el Sars-CoV-2, el último integrante de la familia de los coronavirus, obligó a De Arruda a reorganizar la rutina de trabajo de su grupo de investigación para estudiar cómo actúa el nuevo patógeno en el organismo humano y buscar formas de combatirlo.
En la entrevista que se lee a continuación, que concedió en el mes de enero por videoconferencia, el virólogo, coordinador del Laboratorio de Patogénesis Viral de la Facultad de Medicina de la Universidad de São Paulo en Ribeirão Preto (FMRP-USP), habla de la sorprendente capacidad de propagación del Sars-CoV-2, del surgimiento de nuevas cepas y del riesgo que estas representan con respecto a la eficacia de algunos tipos de vacunas contra el covid-19. También advierte sobre la necesidad de crear sistemas de monitoreo más activos para detectar virus que, eventualmente, podrían desencadenar nuevas pandemias.
Los coronavirus son viejos conocidos suyos. ¿Cuándo comenzó a estudiarlos?
Me decidí a estudiar los virus respiratorios tan pronto como me gradué. Deseaba adquirir un mayor conocimiento sobre los rinovirus, causantes de los resfríos comunes, los agentes infecciosos que afectan con mayor frecuencia a los seres humanos. En aquella época, no era mucho lo que se sabía sobre los rinovirus y fui a trabajar con un grupo de investigación que los estudiaba en la Universidad de Virginia (EE. UU.). También debíamos mantenernos atentos a las variedades de coronavirus que se conocían por entonces, porque se los consideraba la segunda causa del resfriado común en frecuencia. Estos virus son los causantes de aproximadamente el 10 % de las infecciones respiratorias infantiles, una cifra alta. Al final de la década 1980, incluimos el rastreo de los coronavirus en los pacientes con resfríos y, desde entonces, estos virus han estado en nuestra mira.
¿Hay estudios recientes?
En 2019 publicamos el resultado de un estudio realizado con 236 niños atendidos en el Hospital de Clínicas de la USP en Ribeirão Preto. Entre los más de 200 virus estudiados, los coronavirus, por sí solos o asociados con los rinovirus C, fueron los causantes de las infecciones más graves, que requerían de internación en UTI [Unidad de Terapia Intensiva] pediátrica con mayor frecuencia. En ese trabajo fueron estudiados tan solo dos de los cuatro coronavirus que ya eran endémicos en humanos, conocidos por las siglas OC43, 229E, HK11 y NL63.
Usted que los conoce desde hace tanto tiempo, ¿se imaginaba que el Sars-CoV-2 podía causar una pandemia?
Cuando aparecieron las noticias sobre el nuevo virus en China, en diciembre de 2019, pensé que asistiríamos a algo similar a lo que ocurrió en 2002 con el Sars-CoV, causante del Síndrome Respiratorio Agudo Grave, o en 2012, con el virus del Síndrome Respiratorio de Oriente Medio (Sars y Mers, respectivamente, por sus siglas en inglés), que quedaron restrictos al sudeste asiático y a Oriente Medio, en uno y otro caso. Resultó sorpresivo que el nuevo coronavirus se haya propagado como un reguero de pólvora.
¿No había indicios de semejante potencial?
Los virus del Sars y del Mers causaron una enfermedad grave, pero su transmisibilidad era baja. Todos ellos son muy similares en cuanto a su origen zoonótico. Son consecuencia de lo que en inglés se denomina spillover, un salto desde una especie animal al ser humano. Los que nos han enseñado los coronavirus endémicos, y ahora se está confirmando, es que la respuesta inmunológica de los anticuerpos contra ellos es débil. Esto ya se sabía desde la década de 1960, cuando el virólogo británico David Tyrrell [1925-2005], el descubridor de los coronavirus, inoculó esos virus en la nariz de voluntarios sanos. Estos desarrollaron un resfriado y produjeron anticuerpos contra el virus. Un año más tarde, Tyrrell los infectó nuevamente con el virus y comprobó que los anticuerpos prácticamente ya no existían.
¿Existe el riesgo de que esa característica perjudique la eficacia de las vacunas?
Para responder a esta pregunta debo retroceder un poco. La respuesta inmune puede dividirse en dos frentes: uno al mando de las células denominadas linfocitos B y otra por los linfocitos T, que interactúan e intercambian información. Los primeros producen anticuerpos, mientras que los segundos, tras un primer contacto con el virus, son capaces de reconocer a las células infectadas por este. Un subconjunto de linfocitos T, los T CD8, pueden eliminar a las células que contienen virus. La inmunidad que proporcionan los linfocitos T de memoria es más duradera que la de los anticuerpos. Toda esta introducción la hice para poder llegar ahora a la respuesta: sí, la forma en que los coronavirus despiertan la respuesta inmunitaria de los anticuerpos, que es de corta duración, puede perjudicar la eficacia de algunas vacunas.
¿Cuáles pueden verse afectadas?
La mayoría de las vacunas fueron diseñadas tan solo para producir anticuerpos contra la proteína de la espícula, la proteína S del virus. Este es el caso de las vacunas de ARN, tales como la de Pfizer-BioNTech y la de Moderna, o aquellas que utilizan otro virus para introducir en el organismo la fórmula para fabricar la proteína de la espícula del Sars-CoV-2, como en el caso de la vacuna de la Universidad de Oxford/AstraZeneca. Estas vacunas son más proclives a perder eficacia porque la proteína de la espícula, presente en la superficie del virus, puede sufrir mutaciones y, en algún momento, deja de ser reconocida por los anticuerpos inducidos por las vacunas. A medida que los virus se multiplican, su material genético se replica y puede incorporar errores; de eso se tratan las mutaciones mencionadas. Algunas pueden causar alteraciones en las proteínas y tornarlas irreconocibles para un sistema inmunológico expuesto a una versión anterior del virus. Desde el punto de vista evolutivo, la tendencia indica que el virus sufrirá adaptaciones y se volverá menos nocivo para el hospedante. Esto sucede porque el mismo pasa por una selección natural darwiniana. Las variantes que no matan al hospedante o causan una enfermedad más leve se multiplican con más éxito y tienen mayores posibilidades de transmitirse y, como consecuencia de ello, pueden tornarse endémicas. Esto es lo que venimos observando permanentemente en los estudios con células y en animales. Por razones selectivas, hay más probabilidades de que se produzcan mutaciones en la proteína de la espícula, algo que, por cierto, ya está ocurriendo.
Desde el punto de vista evolutivo, la tendencia indica que el virus sufre adaptaciones y se torna menos nocivo para el hospedante
¿Cuál vacuna elegiría para inocularse?
Si pudiera elegir, tomaría una vacuna elaborada con el virus entero, como es el caso de la CoronaVac, producida por la empresa china Sinovac en asociación con el Instituto Butantan, o la Covaxin, de la empresa india Bharat Biotech. Estas vacunas son algo “brutas”: están hechas con trozos del virus tratado con detergente y formalina. Ellas contienen todos los elementos del virus, al igual que la vacuna de la gripe. Ya conocemos el tipo de respuesta inmunológica que generan. El organismo, especialmente a través de las células T de memoria, se vuelve capaz de identificar varias partes del virus, no solo la espícula. Es mucho más fácil que se produzcan mutaciones en una única proteína que simultáneamente en varias de ellas. Asimismo, las vacunas producidas con virus completos inactivados generan una respuesta celular, de los linfocitos T, más duradera. Estudios realizados en Europa y en Estados Unidos han demostrado que entre el 40 % y el 50 % de las personas que nunca estuvieron expuestas al Sars-CoV-2 contaban con linfocitos T capaces de destruirlo, probablemente porque estas células ya habían mantenido contacto con los coronavirus endémicos y pudieron reconocer segmentos que son muy similares en el nuevo coronavirus.
¿Esto significa que una vacuna hecha con el virus entero inactivado puede generar una respuesta inmune más robusta y duradera que una vacuna de ARN, aunque su eficacia sea menor?
Exactamente. Las vacunas fueron diseñadas para prevenir las enfermedades, no para evitar la infección. Un ejemplo clásico es el de la vacuna contra el rotavirus, que prácticamente eliminó los casos de diarrea aguda causada por este virus, pero no impide la infección. Quien recibe una vacuna de virus entero contra el Sars-CoV-2 incluso puede contagiarse, pero probablemente no se enfermará y ni siquiera sabrá que fue infectado. Hubo una alharaca innecesaria en lo inherente a la eficacia de la CoronaVac, que aparentemente es muy buena, porque evita la muerte y previene hasta un 80 % de los casos graves y un 50 % de las manifestaciones leves. Una vacuna que estimula la producción de anticuerpos solamente contra la espícula del virus puede perder eficacia si prevalece un linaje con la espícula alterada.
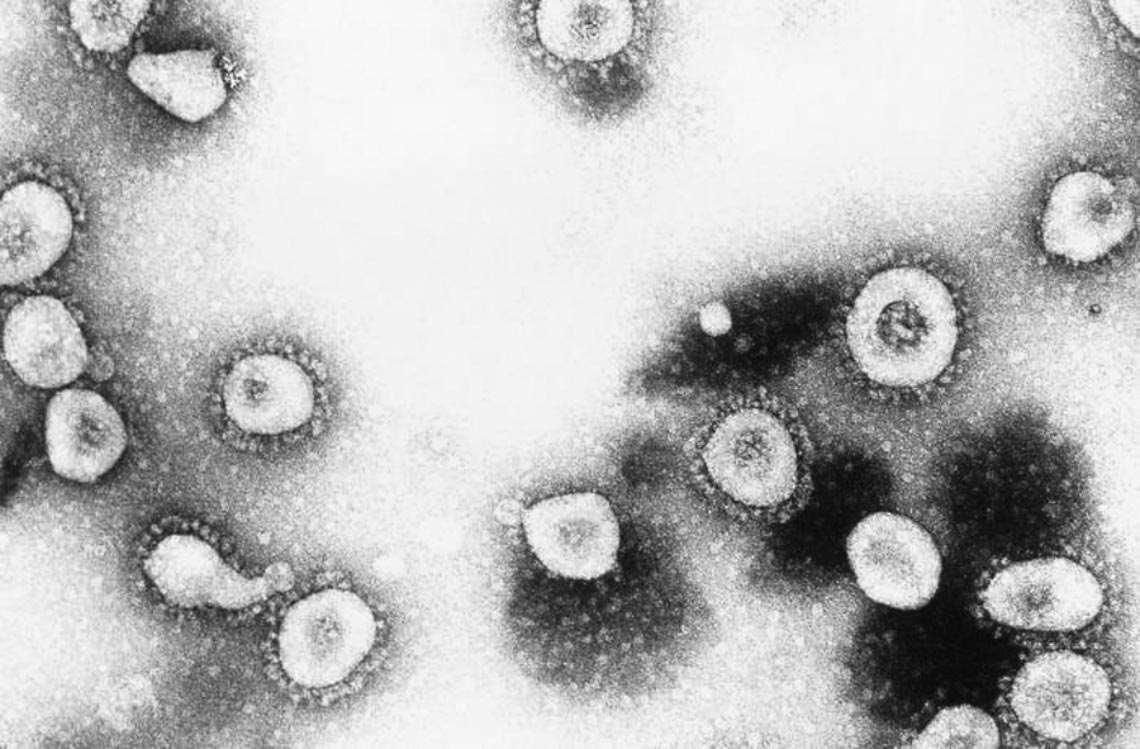
Erskine Palmer / CDC
Copias del coronavirus endémicoErskine Palmer / CDCEl surgimiento de variantes demuestra la importancia de monitorear los virus circulantes. ¿Eso se ha hecho de manera adecuada?
No. Tendríamos que hacer un esfuerzo para recoger más muestras y secuenciar el material genético de este virus mucho mayor que el que se viene haciendo, principalmente en Brasil. Algunos países hacen mucha secuenciación y saben cuáles son las cepas circulantes del virus. Aquí todavía no hacemos esto en la cantidad necesaria. Hay grupos que están secuenciando bastante en los estados de São Paulo, Río de Janeiro, Amazonas y Rio Grande do Sul, pero deberíamos hacerlo en mayor cantidad y con una mejor distribución. No sirve de nada secuenciar todos los virus de São Paulo y ninguno en Mato Grosso, por ejemplo. Deberíamos contar con puestos de vigilancia distribuidos por todo el país para recolectar esas muestras y secuenciarlas para poder seguir la difusión de las variantes. También se necesitan realizar las pruebas para monitorear si esas cepas son capaces de burlar a los anticuerpos inducidos por las vacunas.
¿Este riesgo de fuga hace más urgente la vacunación de la población?
Claro, hay que vacunar a una cantidad muy grande de personas rápidamente para evitar que esas variantes se propaguen, porque cuanta más gente se infecte antes de ser inmunizada, más va a replicarse el virus, acumulando mutaciones y generando nuevas variantes.
Hay indicios de que algunas variantes se propagan con mayor rapidez. ¿Se han realizado estudios que lo confirmen para algunas de ellas?
Excepto por la evidencia de una mayor transmisibilidad en un modelo animal que se obtuvo para la mutación denominada D614G, aún no se ha comprobado con certeza que las variantes que están surgiendo sean más transmisibles. Por el momento, existen evidencias de que algunas producen mayores cantidades de virus en las secreciones, lo que las haría más fácilmente transmisibles. Por eso es que algunos gobiernos dispusieron medidas preventivas, impidiendo el ingreso de viajeros provenientes de los lugares donde existe circulación de esas variantes. Pero todavía no puede afirmarse que todas sean realmente más transmisibles. Se realizaron estudios que utilizan el modelado molecular por computadora que sugieren una transmisibilidad mayor. Pero esto debe verificarse en experimentos de laboratorio. Los estudios de transmisibilidad generalmente se hacen en ratones. Se coloca a un animal infectado en una jaula y se comprueba si contagia a un congénere sano que se encuentra en una jaula vecina, con la cual comparte el aire que respira. Sin estos experimentos resulta imposible saber, por ejemplo, por qué una cepa específica se está esparciendo tanto, como es el caso de la de Manaos. Podría ser que se transmita con mayor facilidad, pero también puede que allí sea más abundante solo porque surgió en esa ciudad, donde ahora ya casi no circularía la cepa que causó la primera ola.
Recién a comienzos de este año China autorizó la entrada en su territorio de un equipo de la Organización Mundial de la Salud para investigar el origen del nuevo coronavirus. ¿Por qué es tan importante saber en qué animal surgió y cómo llegó a los seres humanos?
Para conocer cómo ocurre un spillover y para buscar formas de evitar que ocurran otros. Los spillovers son una consecuencia de la degradación ambiental generada por la actividad humana. Es necesario mitigar los daños conociendo, por ejemplo, cuáles son las especies de murciélagos que antes vivían en los bosques, su ambiente natural, y ahora proliferan en las ciudades. Los murciélagos están presentes en el planeta desde hace más de 60 millones de años y constituyen un reservorio de muchos virus sin llegar a enfermarse porque poseen un sistema inmunológico que no produce demasiada inflamación. Si por medio de estudios genéticos e informáticos podemos conocer cuáles son los virus que portan estos animales y la afinidad de los mismos por las proteínas de las células humanas, es posible estar alerta, intentar evitar el contagio y preparar con antelación medidas de prevención y tratamiento.
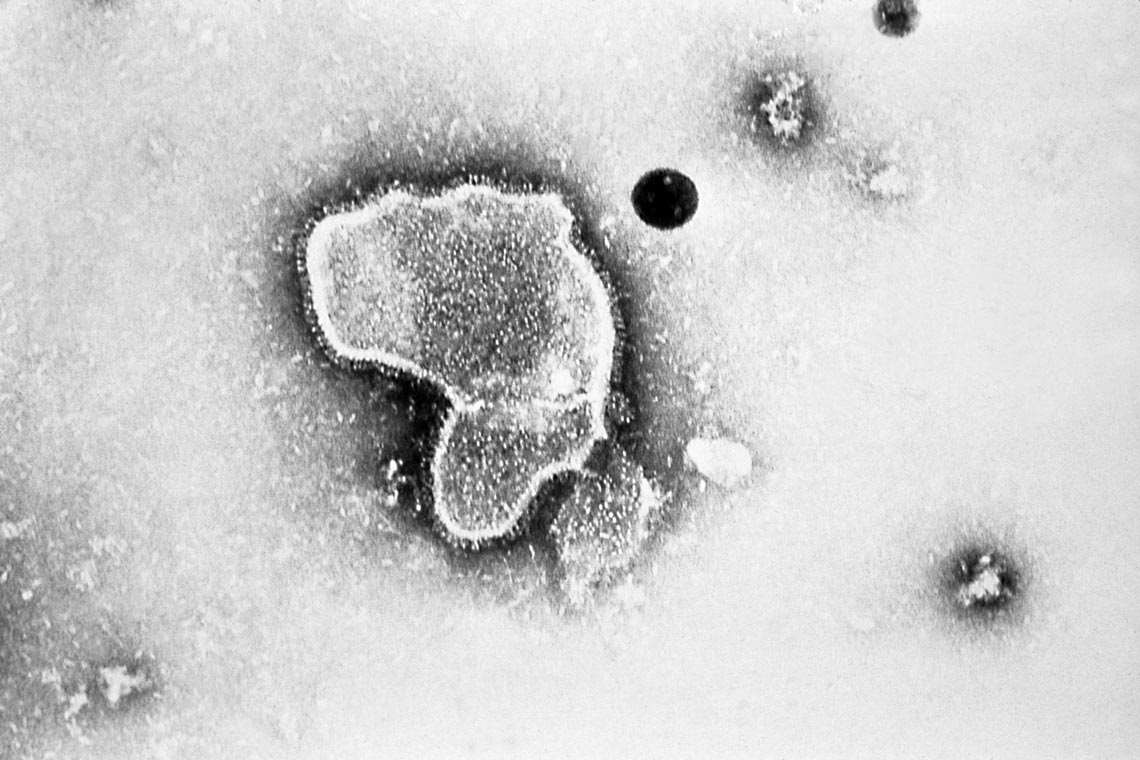
Erskine Palmer / CDC
Un ejemplar del virus respiratorio sincicial humanoErskine Palmer / CDC¿Cuáles son los centros que efectúan cabalmente esa vigilancia zoonótica?
Son muy pocos. Uno de los principales se encuentra en la escuela Médica Duke-NUS, en Singapur. En Estados Unidos existen algunos, tales como el de Galveston, en el estado de Texas, y el de la Universidad de Tulane, en Nueva Orleans. En Brasil, lamentablemente no existen instituciones que realicen una labor centrada en ese aspecto. Tenemos instituciones de salud pública muy buenas, como son el Instituto Evandro Chagas, en el estado de Pará, la Fundación Oswaldo Cruz, en Río de Janeiro y en otros estados, y el Instituto Adolfo Lutz, en São Paulo. Pero están sobrecargados con las tareas cotidianas como para poder encargarse de la prospección de los virus.
¿Cuáles fueron los aciertos y los errores de China y otros países al darse cuenta de que se enfrentaban a un virus peligroso?
No distingo ningún error garrafal en la actitud de los chinos. Aislaron el virus, secuenciaron el material genético y compartieron la información. Al principio, todo el mundo observaba con recelo la propagación del virus, pensando: “¿llegará acá realmente?”. Llegó nomás. En Brasil, las medidas drásticas debieron haberse tomado ni bien apareció, tales como el rastreo en los aeropuertos, la restricción de los viajes y otras disposiciones. Pero es difícil. Hay presiones políticas y económicas. La difusión de noticias falsas fue un gran obstáculo, sugiriendo, por ejemplo, que la cloroquina o la ivermectina podían utilizarse para tratar la enfermedad. Ahora siento miedo por la divulgación de noticias falsas sobre las vacunas. Hay gente que dice que no va a inmunizarse aunque le ofrezcan la vacuna.
¿Hay motivos para preocuparse por los casos de reinfección?
Todos los virus que suscitan en el organismo una inmunidad precaria, como los coronavirus, pueden causar reinfecciones. En la década de 1960, David Tyrrell demostró que eso podía suceder. Lo que me sorprende en el caso del nuevo coronavirus es que las reinfecciones se están registrando en un intervalo de tiempo muy breve, de 60 días, 45 días, y así. Sospecho que algunos de esos casos, en realidad, podrían ser cuadros de persistencia del virus en el organismo.
Las vacunas fueron concebidas para prevenir las enfermedades, y no para evitar la infección. Un ejemplo clásico es el de la vacuna contra el rotavirus
¿Cómo funciona la persistencia?
Hace algunos años empezamos a estudiar las tonsilas [amígdalas] extirpadas a los niños que presentaban hipertrofia en las mismas. Esto causa problemas respiratorios e incluso deformidad facial. Sin embargo, los niños no tenían síntomas de gripe ni de resfriado al momento de la cirugía o durante el mes previo. Analizamos esas amígdalas en el laboratorio y comprobamos que en el 97 % de los casos estaban infectadas con uno o más virus respiratorios. Hallamos material genético y proteínas de varios virus en su tejido. Cuando las maceramos y pusimos ese material en cultivo celular, los virus comenzaron a multiplicarse. Luego de eso, otros grupos de investigación revelaron lo mismo. Recientemente hemos comenzado a estudiar otros tejidos linfáticos –amígdalas, bazo, ganglios linfáticos, timo y médula ósea– de personas que habían fallecido debido a problemas cardiovasculares. Aunque esos individuos no habían muerto a causa de problemas respiratorios, detectamos virus respiratorios, tales como rinovirus, el virus respiratorio sincicial, el virus de la gripe y otros, en varios de esos órganos.
¿Qué revela eso?
Que probablemente esas hayan padecido una infección respiratoria viral en el pasado, estuvieron resfriados, tosieron, estornudaron, y el sistema inmunológico resolvió la infección. Pero el virus halló nichos que podía habitar sin causarle daños al hospedante. Estamos investigando en qué condiciones podría reactivarse la infección. Creo que esta situación en la que el virus convive con su hospedante sin enfermarlo puede ser ventajosa para ambos. Para el virus, porque se mantiene viable durante largos períodos de tiempo, y para el organismo, porque la persistencia viral puede servir como estímulo de la memoria inmunológica sobre cómo combatir la infección.
¿Solo mediante la secuenciación del material genético de los virus en ambos momentos y luego comparándolos puede saberse si se trata efectivamente de una reinfección o si se está ante una infección persistente?
Exacto. No dudo de la posibilidad de reinfección, pero creo que hay que ser más rigurosos al documentarlo. Algo que todavía no se ha detectado en el caso del nuevo coronavirus pero que puede llegar a ocurrir es la recombinación. Si una misma célula se infecta con dos cepas diferentes, el material genético de cada una de ellas puede mezclarse dando origen a una tercera.
Desde el inicio de la pandemia usted orientó a su laboratorio al estudio del nuevo coronavirus. ¿Qué ha descubierto su grupo?
Hasta ahora, nuestro hallazgo más importante fue que el nuevo coronavirus infecta a las células de defensa: monocitos, linfocitos B, linfocitos T CD4 y, para mi asombro, incluso a los linfocitos T CD8. Todas estas células están involucradas en la lucha contra el virus. Algunos virus, como en el caso del VIH, infectan a los linfocitos, pero no se sabía que los coronavirus también fueran capaces de esto.
El Sars-CoV-2 infecta a los linfocitos encargados de combatirlo y también a los que se ocupan de otros patógenos
¿Cuáles son las consecuencias?
Los linfocitos son células que combaten las infecciones en varios tejidos. Si el virus infecta y mata a los linfocitos, ello puede dañar la respuesta inmune. Pero el Sars-CoV-2 no solo infecta a los linfocitos encargados de combatirlo. También ataca a los linfocitos que se ocupan de otros patógenos, lo que podría facilitar otras infecciones. Desde el comienzo de la pandemia, se observó que los pacientes con covid-19 moderado y grave presentan linfopenia, que consiste en un descenso de los linfocitos en la sangre. La causa era desconocida. Se pensaba que esa merma se producía porque los linfocitos habían migrado hacia los tejidos infectados. Demostramos que el virus también mata a los linfocitos, algo que puede generar otra repercusión importante. La respuesta inflamatoria intensa que se observa en el covid-19 puede deberse a la infección de ciertos clones de linfocitos por el Sars-CoV-2. Esto provocaría que dichos clones secretasen una enorme cantidad de citoquinas. Todavía no tenemos prueba de ello.
¿Qué más han visto?
En otro trabajo, colaboramos con el grupo de Fernando Cunha, de la Facultad de Medicina de la USP en Ribeirão Preto, para demostrar que el Sars-CoV-2 induce a otro tipo de células de defensa, los neutrófilos, a liberar trampas extracelulares, las neutrophil extracellular traps, denominadas comúnmente Net. Cuando estas células padecen estrés, como en el caso de la infección por el virus, emiten hacia el medio exterior marañas de su propio ADN que, en el caso de las infecciones por bacterias y hongos, acabarían atrapando a los patógenos. Las Net son muy tóxicas y pueden generar inflamación. Notamos que ellas intervienen en la respuesta inflamatoria en el covid-19. Los pulmones de un paciente que fallece está atiborrado de ellas en los sitios donde hay presencia del virus. Esta comprobación abrió una perspectiva para intentar disminuir la inflamación pulmonar. Existen tratamientos inhalatorios que se basan en el uso de enzimas llamadas ADNasas para disolver las Net. En otro estudio, realizado con Norberto Peporine Lopes, de la Facultad de Ciencias Farmacéuticas de Ribeirão Preto, pudimos observar, recurriendo al modelado por computadora, que la molécula del fumarato de disoproxilo de tenofovir, un antiviral que se utiliza contra el VIH, se encajaba muy bien en la polimerasa del Sars-CoV-2. Esta enzima interviene en la multiplicación del material genético del virus. En experimentos con células, demostramos que el tenofovir redujo en cientos de veces la cantidad del virus. Le informamos del resultado al Ministerio de Salud y conseguimos iniciar un ensayo clínico, actualmente en curso, en Ceará, para verificar si reduce la carga viral, la necesidad de internación y la gravedad de la enfermedad. Con el grupo de Dario Zamboni, constatamos que el virus, al invadir las células del sistema inmunológico, activa en el interior de ellas la formación de un complejo multiproteico denominado inflamasoma, que dispara la respuesta inflamatoria.
¿Cómo surgió su interés por los virus?
En 1981 cuando cursaba el sexto año de la carrera de medicina en la UFC, ya me interesaba la bioquímica de los virus. Un día conocí a una profesora de medicina social, quien me contó sobre un proyecto de investigadores de la Universidad de Virginia, en Estados Unidos. Ellos estaban llevando a cabo un estudio de las enfermedades infecciosas, entre ellas las virales, en la favela de Gonçalves Dias, en Fortaleza. Busqué al coordinador del estudio, Richard Guerrant, y le comenté que iba a estudiar las enfermedades infecciosas para convertirme en virólogo. Él aceptó mi participación y efectuamos un estudio muy cuidadoso. Durante dos años, visitamos las casas de la gente tres veces por semana para constatar si los niños menores de 5 años presentaban síntomas de enfermedades y extraer material para analizarlo en el laboratorio. Conseguí recolectar una buena cantidad de material e identifiqué algunos virus. Durante mi doctorado, realizado en la Unifesp, obtuve una beca para terminar de analizar ese material recolectado en Fortaleza en el laboratorio de virus respiratorios de la Universidad de Virginia.
¿Y qué encontró?
Analizamos un conjunto de virus respiratorios detectados en aquellos niños. El rinovirus, que causa el resfriado, fue el campeón de todos ellos, siendo cinco veces más habitual que el resto. Yo me había graduado en medicina, pero no había estudiado este tema, porque no se lo consideraba un problema de salud importante. Pero lo es. La infección por rinovirus puede desencadenar crisis de asma, sinusitis y otitis media. El 50 % de los pacientes que acuden a una emergencia para tratar las crisis asmáticas están infectados por rinovirus. Hoy en día, se cree que esas crisis son causadas por la respuesta del sistema inmunológico a esos virus. Una vacuna contra rinovirus podría disminuir en un 50 % las crisis asmáticas. En aquel entonces no se sabía casi nada sobre esos virus y me propuse estudiarlos. Mi primer trabajo consistió en demostrar en qué tipo de células se replicaban los rinovirus: las células ciliadas del epitelio respiratorio. Ahora estoy viendo que estos virus también se reproducen en los linfocitos de las amígdalas y de otros órganos del sistema linfático.
¿Por qué resulta tan difícil obtener antivirales eficientes?
Los virus son parásitos bioquímicos complejos. Para mí, son seres vivos, dado que se replican, dejan descendencia y evolucionan. Con la salvedad de que dependen casi por completo de otro ser vivo, en este caso, las células que los hospedan. Como dependen tanto de las vías metabólicas de las células, se necesita hallar compuestos capaces de inhibir la replicación de los virus sin dañar a las células. Y ha sido casi imposible separar las vías que son estrictamente virales de aquellas que son celulares. Existen muchos antivirales, pero no pueden utilizarse. En los experimentos, impiden la proliferación de los virus, pero al comprometer las vías metabólicas de las células, también las matan.

