 Si uno pasa bastante tiempo expuesto a un olor determinado es posible que se torne más eficaz en detectarlo. Puede que esto no parezca sorprendente, e incluso que evoque recuerdos en otros sentidos, como por ejemplo aquellos sonidos tenues que sólo el dueño de casa logra oír e identificar. Pero en el caso del olfato parece haber un mecanismo más determinante, si lo que se observó en ratones vale también para otros animales, el ser humano inclusive. “El andamiaje celular y molecular del epitelio olfativo depende de ciertas pautas genéticas y también se altera conforme a la experiencia de vida”, afirma el biólogo Fabio Papes, docente de la Universidad de Campinas (Unicamp). Junto a colegas del Reino Unido y de Estados Unidos, Papes describió el fuerte componente genético responsable de modular el sistema olfativo, tal como lo describe el artículo publicado el 25 de abril en la revista eLife. Los científicos también detectaron que el órgano sensorial es modificado por el ambiente. Esto es una novedad.
Si uno pasa bastante tiempo expuesto a un olor determinado es posible que se torne más eficaz en detectarlo. Puede que esto no parezca sorprendente, e incluso que evoque recuerdos en otros sentidos, como por ejemplo aquellos sonidos tenues que sólo el dueño de casa logra oír e identificar. Pero en el caso del olfato parece haber un mecanismo más determinante, si lo que se observó en ratones vale también para otros animales, el ser humano inclusive. “El andamiaje celular y molecular del epitelio olfativo depende de ciertas pautas genéticas y también se altera conforme a la experiencia de vida”, afirma el biólogo Fabio Papes, docente de la Universidad de Campinas (Unicamp). Junto a colegas del Reino Unido y de Estados Unidos, Papes describió el fuerte componente genético responsable de modular el sistema olfativo, tal como lo describe el artículo publicado el 25 de abril en la revista eLife. Los científicos también detectaron que el órgano sensorial es modificado por el ambiente. Esto es una novedad.
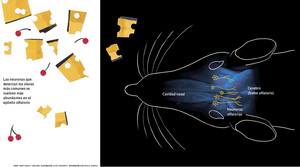
La importancia de la genética en la complejidad del olfato es innegable: más del 5% de los genes presentes en el ADN humano están abocados a producir una diversidad de receptores moleculares que caracterizan a las neuronas olfativas (lea en Pesquisa FAPESP, edición nº 155). Esto significa que el órgano detector de aromas ubicado en el fondo de la cavidad nasal está compuesto por alrededor de 400 tipos de células, cada una de ellas especializada en el reconocimiento de una molécula. “La visión cuenta con tan sólo tres tipos de células”, compara Papes. Se trata de una inversión de fuste, sobre todo si se considera que los seres humanos no tienen al olfato como sentido principal. En el ratón, el modelo utilizado por el profesor de la Unicamp y sus colegas, hay alrededor de mil genes que codifican a los receptores de olores. “Es una de las mayores familias multigénicas que existen”, afirma. Los aromas complejos activan una multiplicidad de receptores químicos, mediante la acción combinada de las células nasales. Esta estrategia de detección es lo que permite identificar un número astronómico de olores (observe la imagen).
Para detallar la contribución de los genes y del ambiente en la formación de este sentido responsable de evaluar la calidad de los alimentos, potenciales parejas sexuales, competidores y depredadores en los alrededores, los investigadores se valieron de dos linajes diferentes de ratones. La particularidad era que todos los representantes de cada una de las familias eran genéticamente idénticos, de manera tal que, a efectos del experimento, funcionaba casi como si el estudio se hiciera en dos individuos diferentes, cada uno con varias réplicas o clones.
En uno de los experimentos, los científicos pusieron en un mismo ambiente a esos ratones y acto seguido compararon el órgano olfatorio de los dos linajes. El grupo del Instituto Sanger, en Inglaterra, bajo el liderazgo del genetista Darren Logan (coordinador del estudio), secuenció el ARN de todo el epitelio olfativo, obteniendo la caracterización más completa hasta ahora de la actividad genética del órgano como un todo. “Es el mayor centro de secuenciación del mundo”, comenta Papes, justificando ese hecho inédito. Así pudo demostrarse que la estructura física de dicho centro de detección de los olores es diferente entre los linajes de ratones incluso en condiciones ambientales estandarizadas, indicando que las células receptoras presentes en cada linaje son consecuencia de diferencias genéticas.
De cualquier modo, el epitelio nasal es cualquier cosa menos algo fijo. “Es uno de los pocos sitios del organismo donde hay neurogénesis constante durante toda la vida”, explica el profesor de la Unicamp. Esta particularidad está relacionada, en parte, con la fragilidad del tejido. Allí, las neuronas se encuentran expuestas al aire externo, contrariamente a las células mejor protegidas del cerebro. Cada vez que ingresan sustancias tóxicas por la nariz –como el humo de una avenida con mucho tránsito vehicular−, las neuronas resultan atacadas y posiblemente llevadas a la muerte. Por eso existe una gran variación a largo plazo: cada célula dura algunos meses, en promedio, antes de ser sustituida.
Sucede que esa sustitución no es aleatoria ni predeterminada, tal como apuntaron los experimentos efectuados en la Unicamp y en el Sanger. Los científicos implantaron embriones de los dos linajes de ratones en hembras sustitutas, de modo tal, de crear un ambiente gestacional controlado y homogéneo, y luego devolvieron las camadas a las madres de cada uno de los linajes, aunque con una singularidad: cada una de las camadas contenía a una cría adoptiva de otro tipo de linaje. El diseño experimental partió del principio de que las madres genéticamente distintas presentan una serie de particularidades en cuanto a cómo influyen sobre la experiencia sensorial de las crías, como el olor de la leche, por ejemplo. Una vez adultos, esos ratones fueron analizados según el grupo al que pertenecían: ejemplares de cada uno de los linajes criados en ambientes que contenían madres similares, y aquellos criados por madres de linaje diferente (vea la infografía).
La manipulación permitió la detección de diferencias sutiles en el perfil de expresión génica del epitelio olfativo en ratones que vivieron situaciones distintas, indicativo de que el ambiente también contribuyó para la construcción del órgano. “Eso era algo que no estaba previsto”, comenta Papes. La detección de esa variación representó un desafío técnico importante, porque cada tipo de molécula aromática afecta a pocas células de la nariz. Esto explica el hecho de que recién ahora se haya realizado un análisis tan minucioso a gran escala, cuando los recursos para efectuar análisis genéticos se tornaron más sofisticados.
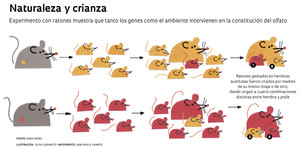 Olfato mutable
Olfato mutable
En los experimentos también se estudiarán más a fondo los cambios que ocuren durante el transcurso de la vida, al exponer a ratones adultos a cuatro moléculas aromáticas cuyas células detectoras son conocidas, como el aroma a banana o a clavo de olor. El aroma estaba presente en el agua disponible para los animales, que sentían el olor cada vez que bebían. Pese a no ser continua, ya que no estaban expuestos permanentemente, fue una exposición prolongada, durante un lapso de seis meses. La secuenciación posterior reveló mayor actividad en ciertos genes, que se interpretó como un aumento en el número de células portadoras de los receptores específicos para los cuatro aromas. Bastaron seis semanas sin agua aromatizada para que los niveles de expresión de los genes retornaran a lo normal.
“Esta fue la primera vez que se calculó de manera abarcadora que la cantidad de neuronas olfativas que expresan cada uno de los mil tipos de receptores olfativos varía entre los diferentes linajes de ratones”, pondera la bioquímica Bettina Malnic, del Instituto de Química de la Universidad de São Paulo (IQ-USP), una de las mayores especialistas en neurobiología del olfato en Brasil. Ella no participó del estudio, pero tiene especial interés en la genética inmanente tras las neuronas olfativas y en cómo se regula la expresión de esos genes (lea en Pesquisa FAPESP, edición nº 220), tal como revela una revisión reciente en la revista Molecular Pharmacology.
Fabio Papes/ Unicamp
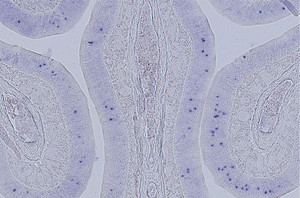
El epitelio olfativo de los ratones permite el contacto directo entre el aire y las neuronas (los núcleos son los puntos oscuros)Fabio Papes/ UnicampVida y muerte
En un estudio cuyos resultados fueron remitidos para su publicación, el grupo de Malnic utilizó ratones genéticamente alterados, que no lograban transmitirle a su cerebro las señales relativas a los olores, y detectó que ante esa eventualidad las neuronas del epitelio olfativo sucumben. “La incapacidad para responder a los olores incide en la supervivencia de las células”, explica, aunque ella aún no ha encontrado la vía bioquímica que determina dicha muerte celular. Constantemente se producen nuevas células, pero la alta mortalidad hace que el epitelio olfativo de esos ratones modificados esté compuesto por un número reducido de neuronas. “El incremento que esos investigadores observaron en la expresión génica de los ratones criados en ambientes donde se agregó un aroma específico es compatible con la idea de que hubo un aumento en la sobrevida de las neuronas activadas por el olor”, sugiere.
Mientras llevaba adelante su investigación, para Malnic fue una grata sorpresa encontrar el artículo de Papes y sus colaboradores antes de su publicación oficial, en el repositorio electrónico de preprints bioRxiv (lea en Pesquisa FAPESP, edición nº 254). “El acceso a los resultados del estudio incluso antes de su publicación definitiva contribuyó para lograr un mejor delineamiento de los experimentos que ya estaban en curso en mi laboratorio”, relata.
Las preguntas que surgen a partir de las nuevas respuestas garantizan trabajo de sobra para los dos grupos en los próximos tiempos. Más allá de profundizar el estudio de los posibles mecanismos para el incremento en la frecuencia de los receptores más usados, tales como la longevidad de las células y la regulación de la actividad génica, también resta analizar cómo esa variación a lo largo de la vida y entre individuos puede alterar la percepción del ambiente. Papes sugiere que en los otros sentidos podría existir una plasticidad similar, dado que aún no han sido estudiados desde esa misma perspectiva.
Los resultados sugieren un mecanismo adaptativo, que se suma a lo que ya se sabía sobre la memoria sensorial (cuando un aroma evoca un recuerdo específico) y la habituación (cuando la exposición frecuente a un estímulo provoca que se desconecten las neuronas del cerebro involucradas con su interpretación). “Describimos una nueva estrategia adoptada por el organismo, donde los factores ambientales alteran el modo en que se constituye el órgano olfativo, adaptando al individuo para la vida en ese ambiente”, dice Papes.
El investigador también visualiza un gran impacto en la medicina personalizada. “Si los sentidos son distintos para cada individuo, no sólo porque sus fisiologías son diferentes, sino también porque la propia constitución celular de sus órganos sensoriales no es idéntica, entonces debemos considerar único a cada ser humano desde un punto de vista sensorial”, afirma. Desde esa perspectiva, sostiene que podrían desarrollarse fármacos para tratar trastornos sensoriales o modelar los comportamientos causados por ellos en ciertos grupos específicos de personas.
En las últimas dos décadas, relata, en una serie de estudios se está investigando hasta qué punto influye el olfato en el comportamiento humano, como en los casos de la relación entre la atracción sexual y los olores corporales. Los hallazgos actuales sugieren que los nuevos abordajes genéticos podrían contribuir para una mejor comprensión. Uno de los proyectos en curso en el Instituto Sanger involucra a un experimento a gran escala entre la población inglesa para secuenciar el ARN del órgano olfativo, mapear genéticamente su epitelio y determinar la correspondencia de los genes con diferentes tipos de enfermedades y trastornos sensoriales involuntarios. Papes espera poder participar, incluyendo muestras brasileñas entre la población secuenciada. “La diversidad social y la variabilidad genética en Brasil torna a nuestra población especialmente interesante para este tipo de estudios”.
Artículos científicos
IBARRA-SORIA, X. et al. Variation in olfactory neuron repertoires is genetically controlled and environmentally modulated. eLife. v. 6, e21476. 25 abr. 2017.
NAGAI, M. H. et al. Monogenic and monoallelic expression of odorant receptors. Molecular Pharmacology. v. 90, n. 5, p. 633-9. nov. 2016