Una segunda generación modificada de la proteína spike del nuevo coronavirus, el Sars-CoV-2, causante del covid-19, forma parte de una nueva candidata vacunal que recientemente entró en la fase de ensayos clínicos en humanos en Estados Unidos, Vietnam y Tailandia. El agente inmunizante en cuestión, cuya denominación genérica es NDV-HXP-S, fue desarrollado mediante una colaboración internacional para su producción en las instalaciones de países en desarrollo, que actualmente se emplean para elaborar la vacuna de la gripe en huevos embrionados, y su almacenamiento en los mismos sistemas convencionales de refrigeración que se utilizan para conservar la mayoría de las vacunas para otras enfermedades.
La proteína de la superficie del nuevo coronavirus, la ya mencionada spike, es la responsable de unirse a los receptores en la superficie de las células humanas y desencadenar la infección por el Sars-CoV-2. Es por eso que se la utiliza habitualmente como antígeno en las vacunas contra el covid-19, es decir, como el elemento extraño que reconoce el sistema inmunológico y que oficia como blanco para la producción de anticuerpos abocados específicamente a combatir a un patógeno. La HexaPro, tal como se denomina a la segunda versión modificada de la spike, es una versión mejorada de la representación tridimensional de esa proteína. Según sus creadores, esta es más estable y fácil de conservar que su versión anterior, la 2P.
En Brasil, la única vacuna en desarrollo a partir de la HexaPro es la llamada ButanVac, que será producida por el Instituto Butantan, de São Paulo. A finales del mes de abril, el Butantan inició la producción de un lote de un millón de dosis del producto. El instituto espera contar hacia el 15 de junio con 18 millones de dosis de la ButanVac, que aguarda la autorización de la agencia reguladora Anvisa para el inicio de los ensayos clínicos. La vacuna contiene una variante modificada del virus de la enfermedad de Newcastle, que afecta a las aves y prácticamente es inocua para los seres humanos, y fue desarrollada por el equipo de investigadores de Peter Palese, de la Escuela Icahn de Medicina de la red de hospitales Monte Sinaí, de Nueva York, para producir la HexaPro (lea en Pesquisa FAPESP, edición nº 302).
A excepción de las vacunas que utilizan el coronavirus completo (inactivado o atenuado) como antígeno en sus formulaciones, como es el caso de la CoronaVac que se utiliza en Brasil y la produce el Instituto Butantan, el resto de los inmunizantes emplean únicamente la proteína spike para estimular al sistema inmunológico. Las vacunas de Pfizer/BioNTech, Moderna y Janssen, las tres aprobadas en Estados Unidos, usan la 2P como antígeno, al igual que otra candidata a vacuna de la empresa farmacéutica estadounidense Novavax. La historia de la 2P y la HexaPro comenzó en el mismo lugar.
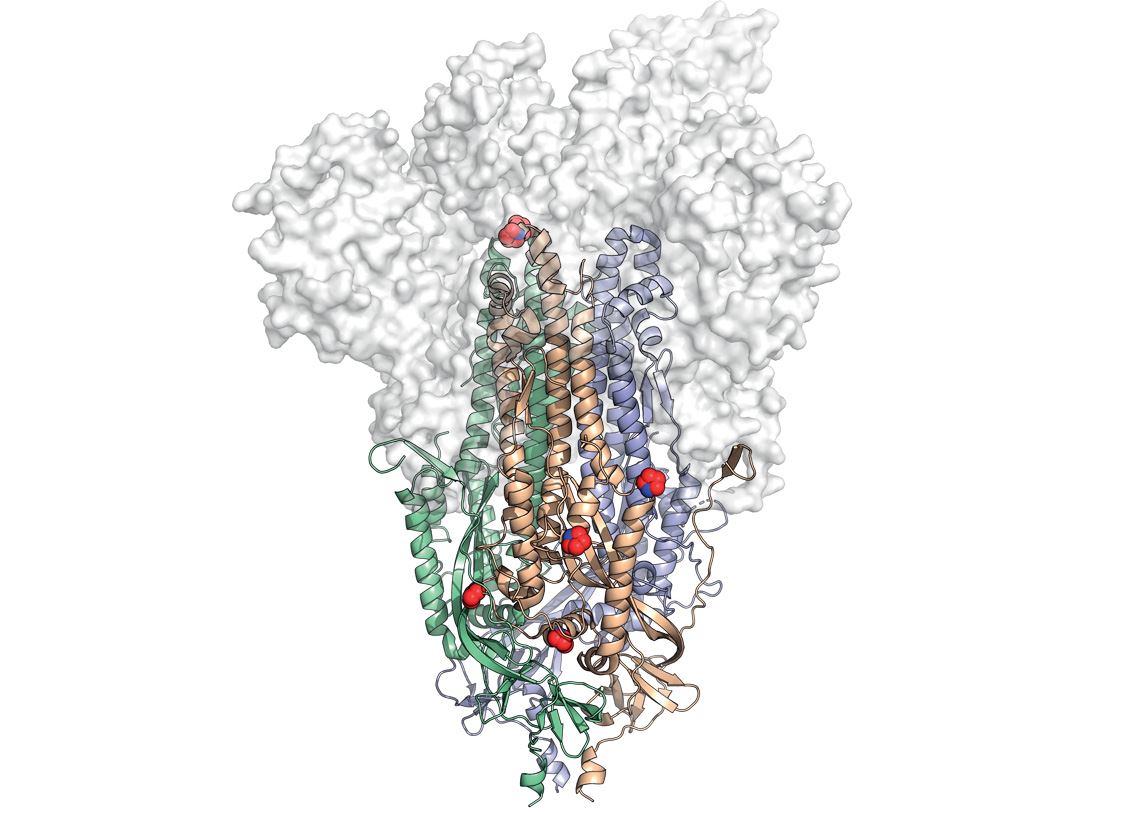
Universidad de Texas en Austin
La estructura de la proteína spike en donde se encuentra marcada la ubicación de las modificaciones (las esferas rojas y azules), que le confieren mayor estabilidadUniversidad de Texas en AustinEn febrero del año pasado, antes que la pandemia del covid-19 se propagara en Occidente, el biólogo estructural estadounidense Jason McLellan, de la Universidad de Texas, en Austin [EE. UU.], describió en un artículo publicado en la revista Science, la primera representación tridimensional estabilizada de la proteína de la espícula del Sars-CoV-2, que luego sería llamada 2P. “Esta proteína es muy inestable antes de que el virus penetre en las células humanas”, explicó McLellan, en una entrevista concedida a Pesquisa FAPESP. “Tenemos que hacerla más estable, recurriendo a modificaciones moleculares, para poder utilizarla como antígeno en una vacuna”.
La 2P contiene dos de esas modificaciones (de ahí proviene su nombre). Se trata del agregado de dos prolinas, un tipo de aminoácidos que torna más rígida a la normalmente variable estructura tridimensional que exhibe la spike antes de invadir las células del hospedante. Las proteínas pueden estar constituidas hasta por 20 aminoácidos diferentes. Los tejidos conectivos más rígidos, como el colágeno, contienen prolinas en abundancia. A los biólogos les gusta comparar el uso de las prolinas para estabilizar a las proteínas con el empleo de ganchos moleculares que procuran mantener al compuesto en una conformación determinada. En el caso de la HexaPro, cuya estructura en 3D fue dada a conocer en julio de 2020 en otro artículo en la revista Science, se introdujeron seis prolinas. Con media docena de ganchos moleculares, esta versión de la espícula es más estable, lo que puede ser útil para generar una mejor respuesta inmunológica, además de permitir la conservación de las vacunas que la emplean como antígeno en un rango de temperatura entre 2 y 8 grados Celsius (ºC). “Pudimos producir rápidamente versiones más estables de la proteína de la espícula del Sars-CoV-2 porque con mis colegas ya estábamos trabajando, antes de la pandemia, con la generación de estructuras en 3D de dicha proteína en otros tipos de coronavirus, tales como el Mers [del Síndrome Respiratorio de Oriente Medio] y el HKU1”, explica McLellan.
La combinación del trabajo del equipo de McLellan con la proteína spike del Sars-CoV-2 y los esfuerzos de los colaboradores de Peter Palese, del Monte Sinaí, para la producción de una versión modificada y de fácil cultivo del virus de Newcastle, condujo al desarrollo de la candidata a vacuna NDV-HXP-S. La colaboración fue impulsada por Path, una organización no gubernamental con sede en la ciudad de Seattle (EE. UU.), que trabaja en pro del empleo de soluciones de salud innovadoras en los países en desarrollo. A causa de la gravedad de la pandemia, tanto el grupo de Austin como el de Nueva York, que poseen las patentes del desarrollo del agente inmunizante, acordaron ceder licencias del producto sin cobrarles royalties a un grupo de países de ingresos medios y bajos, entre ellos, Brasil.
Según informa la comisión de prensa de Path, las versiones de la NDV-HXP-S que se están fabricando para probarlas en diferentes países son comparables. Utilizan un mismo lote de materiales (banco de semillas virales), que fueron reproducidos, purificados e inactivado por métodos similares y formulados en vacunas con un mismo ensayo de potencia. “Por lo tanto, los datos de los ensayos clínicos que se realicen con cualquiera de esas tres vacunas [en alusión a las fórmulas de Tailandia, Vietnam y Brasil] marcarán los resultados esperados para las otras dos”, informa la asesoría, en un correo electrónico enviado a Pesquisa FAPESP.
“Los altibajos forman parte del desarrollo de las vacunas”, dice el biólogo Ricardo Oliveira, director de Producción de la Fundación Butantan (lea el informe intitulado “Camino sinuoso” en el sitio web de Pesquisa FAPESP). Con todo, según Oliveira, “no debería haber mayores dificultades para ampliar la escala de producción” de la ButanVac en el caso de que los ensayos clínicos resulten exitosos. Al fin y al cabo, el inmunizante contra el covid-19 emplea una tecnología ya conocida por el Instituto Butantan que se utiliza para producir la vacuna anual contra la gripe disponible en la red de salud pública de Brasil.
Republicar