Brasil, el mayor exportador mundial de carne vacuna, da los primeros pasos en la carrera por un mercado que ha atraído decenas de millones de dólares en los últimos años: el de productos alternativos a la carne, pero con las mismas características sensoriales. Existen dos caminos posibles para lograr este objetivo: la producción de carne de laboratorio a partir de células madre de animales, también conocida como carne limpia o in vitro, y la creación de un producto a base de proteínas vegetales que emule a la carne roja. En mayo de este año, el empresario de Río de Janeiro Marcos Leta lanzó en el mercado a Futuro Burger, una hamburguesa vegetal que promete tener la apariencia y el sabor de la carne bovina. Fundador de los jugos Do Bem, el empresario es dueño de la foodtech Fazenda Futuro, responsable de la novedad, vendida a unos 17 reales la bandeja con dos unidades.
Leta sigue el camino recorrido por empresas extranjeras que ya venden alternativas vegetales al producto de origen animal, conocidas como plant-based meat (carne de origen vegetal). Los ingredientes de Futuro Burger están formados por proteína aislada de soja, de garbanzo y de arveja. El color rojizo se lo otorga el jugo de la remolacha. Según Leta, no solo en la apariencia los alimentos son similares a la carne de origen animal, sino también en sabor, textura y aroma. En el proceso se utilizó una lengua artificial, un equipo electrónico compuesto por sensores gustativos que imitan el funcionamiento del órgano humano. “El valor nutricional también es muy similar”, dice Leta. Este resultado se obtuvo a través del análisis, con la ayuda de la inteligencia artificial, de las mejores combinaciones de proteínas y lípidos de origen vegetal.
Futuro Burger es la primera hamburguesa vegetal fabricada en Brasil que imita a la carne roja
> Ingredientes
La base del producto consiste en proteína aislada de soja, garbanzos y arvejas
> Aspecto
El color rojizo, imitando a la sangre, le es conferido por el agregado de jugo de remolacha
> Valor nutricional
Con la ayuda de la inteligencia artificial, la empresa investigó la mejor combinación de proteínas y lípidos
> Un mercado en aumento
En Estados Unidos, la venta de productos de origen vegetal similares a la carne alcanzó los 670 millones de dólares en el primer semestre de 2018
> Carne limpia
Además de las hamburguesas veganas, otro camino para crear nuevos productos es invertir en la elaboración de carne a partir de células madre de animales
Además de los vegetarianos, el objetivo es llegar a quienes buscan alimentarse de una manera ecológicamente sostenible. Un estudio publicado por el Observatorio del Clima en 2016 mostró que el sector agropecuario es responsable por el 69% de las emisiones de gases de efecto invernadero en Brasil. “Queremos demostrar que es posible revolucionar la industria alimentaria sin generar impactos negativos en el medio ambiente”, dijo Leta.
Durante el proyecto, la empresa contrató una consultoría de la organización estadounidense The Good Food Institute (GFI), especializada en el desarrollo de proteínas alternativas. “Trabajamos para crear un sistema alimentario más sostenible, saludable y justo. Nuestro equipo de científicos, emprendedores y especialistas en políticas públicas trabaja para que la industria alimentaria utilice productos hechos con plantas o con células animales”, explica Felipe Krelling, coordinador del sector de Innovación e Investigación del GFI en Brasil.
Es una novedad en Brasil, pero la hamburguesa vegetal que imita a la carne bovina existe hace tres años en Estados Unidos. Beyond Burger fue la primera empresa en vender sus hamburguesas a base de vegetales en cadenas de supermercados del país. Este año, se convirtió en el primer fabricante de carne vegetal con acciones en la bolsa de valores Nasdaq, de Estados Unidos. Además de hamburguesas, vende carne molida y salchichas preparadas a través de una combinación de fuentes proteicas vegetales.
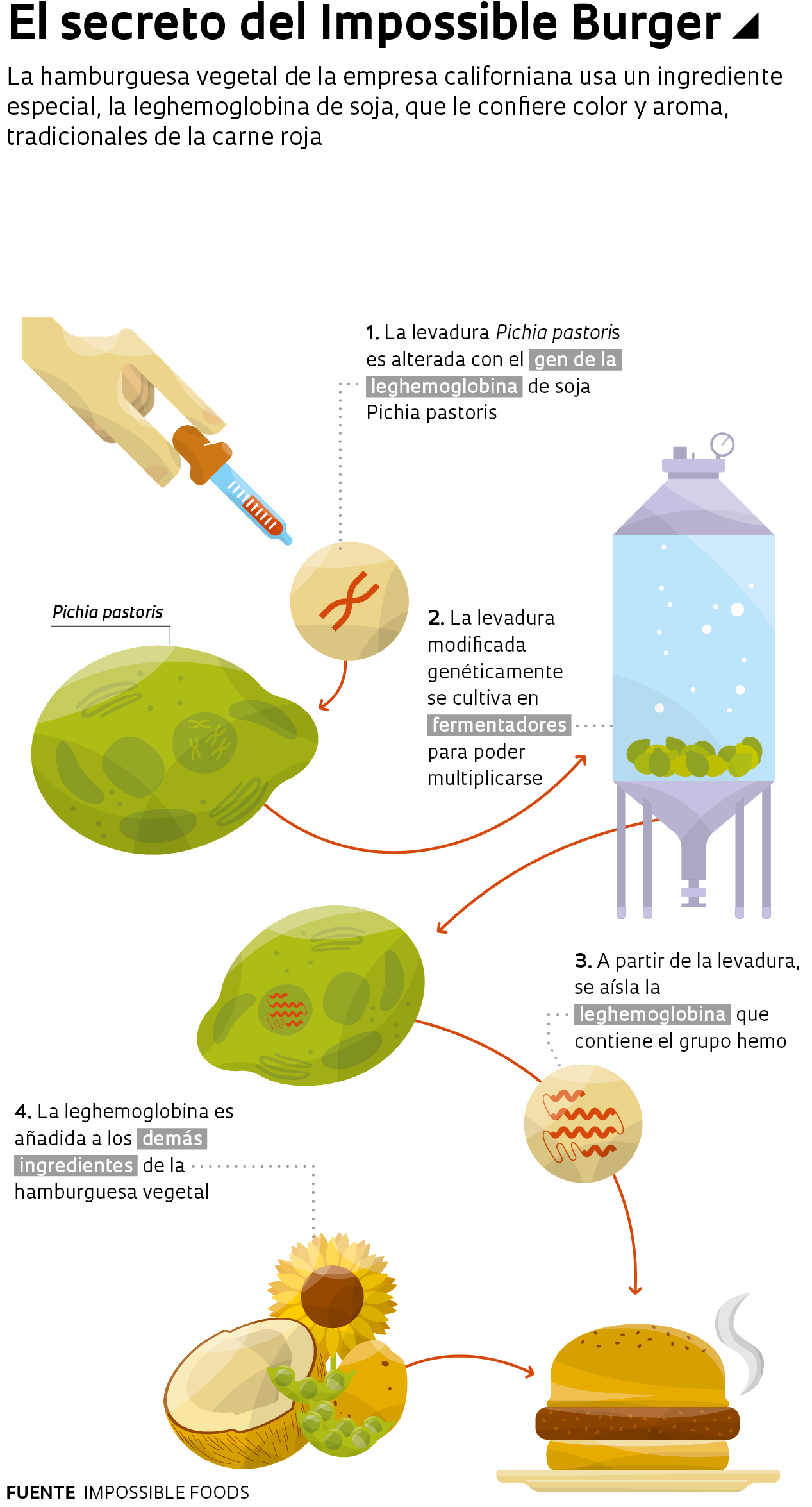
La startup californiana Impossible Foods dio un paso más. El color rojo de su hamburguesa proviene de una proteína similar a la hemoglobina, producida a través de la ingeniería genética. Los investigadores de la empresa utilizan un componente de hemoglobina, el grupo hemo, que le confiere el color rojo de la carne cruda y el olor característico exhalado durante la cocción. Las raíces de las leguminosas poseen el grupo hemo en una proteína con estructura y funciones muy similares a la hemoglobina, la leghemoglobina.
Basándose en estos conocimientos, los científicos de Impossible Foods crearon un método de producción a gran escala del grupo hemo, extrayéndolo de las raíces de la soja. A través de la ingeniería genética, modificaron la levadura Pichia pastoris para que produjera leghemoglobina de soja y la cultivaron en fermentadores que multiplican la proteína.
Aleph Farms/ Divulgación
Equipo israelí de investigación y desarrollo, de la Aleph FarmsAleph Farms/ DivulgaciónHamburguesas in vitro
Los emprendedores que invierten en el cultivo de células madre bovinas para crear carne sintética, también llamada cell-based meat (carne hecha con células), tienen un argumento aún más convincente para atraer a los amantes de un buen bife: lo que hacen no es algo que simplemente se parece a la carne, sino que es la propia carne. La primera hamburguesa in vitro nació en la Universidad de Maastricht, Holanda, a partir de la investigación del fisiólogo Mark Post.
Los estudios comenzaron en 2008 y el resultado fue presentado cinco años después, durante una conferencia de prensa celebrada en Londres. En esa ocasión, tres personas que probaron la hamburguesa –el propio Post y dos especialistas en alimentos– estuvieron de acuerdo en que la carne estaba algo seca y con poco sabor, debido a la falta de grasa en la composición, según le explicaron a The New York Times.
El proceso desarrollado por Post empieza con la extracción de células madre de bovinos, a partir de un fragmento de tejido muscular del animal. Estas células indiferenciadas se multiplican en un medio de cultivo que contiene nutrientes y factores de crecimiento, transformándose en fibras musculares. Alrededor de 20.000 tiras delgadas de tejido muscular se combinan para formar una hamburguesa de unos 140 gramos. La producción a escala industrial se realizará en un biorreactor.

Mosa Meat / Divulgación
Hamburguesa in vitro en la Universidad de Maastricht, en HolandaMosa Meat / DivulgaciónLa hamburguesa holandesa costó 250.000 euros (1,1 millones de reales), fue financiada principalmente por Sergey Brin, cofundador de Google. Con el fin de poner el producto en el mercado, el investigador creó la empresa Mosa Meat, nacida como una spin-off de la Universidad de Maastricht. En julio de 2018, para continuar el desarrollo de productos y empezar su comercialización, la startup recaudó 7,5 millones de euros de Bell Food Group, líder en el mercado de carnes en Suiza, y de la holandesa M Ventures.
A finales del año pasado fue el turno de la israelí Aleph Farms, que anunció la creación del primer bife cultivado en laboratorio. Didier Toubia, CEO de la compañía, le informó a Revista FAPESP que la decisión de investigar la carne cultivada a partir de células animales surgió en 2016. El proyecto se llevó a cabo en la Facultad de Ingeniería Biomédica del Instituto de Tecnología de Israel (Technion).
La primera hamburguesa hecha con células madre se preparó en Holanda y costó 250.000 euros
El costo del prototipo, una pequeña tira de bife de unas pocas decenas de gramos, fue de 50 dólares, todavía bastante caro si se lo compara con el de la carne vendida en las carnicerías, pero un avance en relación al desperdicio generado por la producción de hamburguesas en Maastricht. La novedad llegará al mercado en cinco años, como máximo.
El proceso de producción de un bife in vitro es más complejo y requiere que las células se organicen de forma tridimensional (3D), ganando volumen y consecuentemente espesor. Para ello, es necesario colocarlas dentro de una estructura que sirva como soporte llamada scaffold (andamio), que normalmente se produce con colágeno, de origen animal. Pero para fabricar carne limpia es importante que no haya insumos ni procedimientos animales vinculados al proceso. Estos requisitos previos han estimulado el surgimiento de empresas que presentan nuevas tecnologías. Una de las startups creadas para proporcionar scaffolds a base de hierbas, es la brasileña Biomimetic Solutions, una spin-off nacida en el Centro Federal de Educación Tecnológica de Minas Gerais (Cefet-MG).
“Creamos un polímero sintético a base de hierbas. Somos una de las primeras empresas del mundo especializadas en la producción de scaffolds centrados en la producción de carne limpia”, afirma Lorena Viana, estudiante de maestría en innovación, UFMG, y una de las fundadoras de la startup, conjuntamente con las ingenieras de materiales Ana Elisa Antunes y Alana Benzo, y dos investigadoras de Cefet-MG, Aline Bruna da Silva y Roberta Viana. “Decidimos centrar nuestro negocio en el mercado de la carne in vitro, donde tenemos pocos competidores directos”, dijo Viana, directora comercial del negocio. Mosa Meat y Aleph Farms ya desarrollan sus propios scaffolds.

Con el fin de estimular la agricultura celular, un campo en el que se inserta el desarrollo de carne cultivada en laboratorio, en 2016 se creó en Estados Unidos, la Sociedad de Agricultura Celular (CAS). “En todo el mundo, sólo América Latina aún no ha desarrollado proyectos de carne in vitro“, dice Matheus Saueressig, estudiante de informática de la Universidad Federal de Rio Grande do Sul (UFRGS) y Director de Comunicaciones de la CAS en Sudamérica. “Brasil es el mayor procesador de proteínas animales del mundo y corre el riesgo de perder este nuevo mercado”, advierte.
Las startups dedicadas a la investigación y fabricación de carne limpia, según Saueressig, han estado recibiendo inversiones de empresas de capital de riesgo, de multimillonarios como Richard Branson y Bill Gates, que tienen una participación en Memphis Carne, con sede en California, y multinacionales del sector alimentario, incluyendo Cargill, Bell Food Group y Tyson Foods. Al apoyar a los nuevos fabricantes de carne limpia, los grandes procesadores de carne vacuna quieren poner un pie en este mercado para no quedarse del lado de afuera, en caso de que el negocio funcione.
Por ahora, las alternativas vegetales dominan el prometedor mercado de posibilidades de la carne vacuna. Un estudio de la consultora Nielsen reveló que los estadounidenses consumieron 670 millones de dólares en productos de origen vegetal similares a la carne en el primer semestre de 2018: veganos y vegetarianos representan sólo el 5% de la población del país. Las empresas dedicadas a la producción de carnes a base de células madre aspiran a un mercado mucho mayor. Se espera que la carne bovina represente ingresos de 2,1 billones de dólares en todo el mundo hasta 2020, según la consultora estadounidense Grand View Research.
Desafíos a la vista
Pese a las buenas perspectivas, ya hay reacciones. El término “carne limpia”, por ejemplo, es discutido tanto por veganos como por ganaderos. Los primeros están en contra del uso del adjetivo “limpio” si existe cualquier tipo de uso de células extraídas de animales, mientras que la industria de proteínas animales se opone al uso de la palabra “carne” por temor a la competencia. La Asociación de Ganaderos de Estados Unidos le ha planteado al Departamento de Agricultura que los productos no derivados de animales criados o faenados no se describan como bife o carne. El propósito es diferenciar el alimento que ellos producen, de la novedad que está surgiendo en el mercado. Uno de los mayores retos de las nuevas empresas no es comercial, sino científico: deben garantizar que el proceso de producción no haga uso de ningún componente de origen animal.
En la primera hamburguesa in vitro, Mark Post utilizó suero bovino fetal para nutrir a las células madre. Hoy en día, tanto Mosa Meat como Aleph Farms aseguran que no utilizan más ingredientes derivados de animales. Sin embargo, el veterinario Flávio Vieira Meirelles, de la Facultad de Zootecnia e Ingeniería Alimentaria de la USP (FZEA-USP), sostiene que es muy difícil reemplazar aminoácidos, proteínas, azúcares, vitaminas y factores de crecimiento que se encuentran naturalmente en la sangre animal, por sustancias aisladas de plantas. “Existen alternativas al suero fetal, pero también tienen origen animal. Y hay varias otras sustancias extraídas de animales involucrados en las diferentes etapas del proceso”, dice. “Va a llevar tiempo hasta que se pueda cultivar una célula a escala industrial con un costo viable y que esté completamente libre de productos de origen animal.”
Algunas foodtechs, como las estadounidenses Just y Memphis Meats, invierten para producir carne en el laboratorio sin siquiera hacerle una simple biopsia al animal. Estas empresas utilizan células madre extraídas de plumas de aves para producir carne de pollo. Just vende alimentos vegetales alternativos a los de origen animal, como la mayonesa. Memphis Meats, por su parte, se dedica a investigar varios tipos de carne de laboratorio, incluyendo pollo y pato.

Impossible Foods/ Divulgación
La fábrica de Impossible Foods: inversión en investigaciónImpossible Foods/ DivulgaciónLa misma textura
En 2017 Liz Specht, directora asociada de Ciencia y Tecnología del GFI en Estados Unidos, experimentó la carne de pato, hecha por Memphis Meats a partir de células madre. “Lo que más me impresionó fue la textura. Cuando se muerde una fibra muscular, se nota la elasticidad que le es propia, y la carne a base de células que comí tenía la misma calidad”, dijo poco después del experimento, según informó el GFI. “Era una milanesa y tenía salsa, por lo que fue difícil medir el sabor en sí de la carne, pero la textura era inconfundible”.
Otro desafío para los fabricantes de la carne in vitro es demostrar que el producto es seguro para el consumo humano. “Tendrán que identificar claramente qué sustancias se utilizan en el proceso de diferenciación celular, demostrando seguridad y calidad nutricional”, dice la bioquímica Viviane Abreu Nunes Cerqueira Dantas, de la Escuela de Artes, Ciencias y Humanidades de la USP.
La investigadora ve con recelo la afirmación, común entre las startups del sector, de que la carne de laboratorio, al contrario del producto derivado del sacrificio de animales, no utiliza antibióticos. “Al principio, la producción de carne in vitro a gran escala no será capaz de prescindir del uso de antibióticos para el cultivo celular. Pero desconozco qué otras sustancias se pueden utilizar con ese mismo efecto en el contexto de la producción de carne de laboratorio”, evalúa. Según Dantas, los productos cárnicos, en particular los que se someten a una mayor manipulación, constituyen un excelente medio de cultivo de microorganismos debido a la alta humedad, el pH cercano a la neutralidad y la composición rica en nutrientes.
Felipe Krelling, de GFI, informa que los antibióticos se pueden utilizar durante un corto período para minimizar los riesgos de contaminación al separarse una línea celular de una biopsia, en caso de que esté contaminada por alguna bacteria. “No hay necesidad de usar ningún tipo de antibiótico en otros momentos del proceso de producción. Ya existe una tecnología en la industria de los bioprocesos que puede ser adoptada por empresas cell-based para obtener un ambiente libre de antibióticos para la proliferación celular”, afirma Krelling.
Artículo científico
LYNCH, J. e PIERREHUMBERT, R. Climate impacts of cultured meat and beef cattle. Frontiers in Sustainable Food Systems. 19 feb. 2019.
